Facharzt des Artikels
Neue Veröffentlichungen
Hyperplastische Gastritis: Symptome, Behandlung, Ernährung, Prognose
Zuletzt überprüft: 04.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
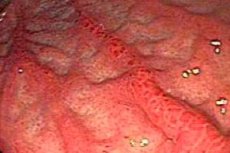
Hyperplastische Gastritis ist eine morphologische Form einer chronischen Magenerkrankung, bei der pathologische Veränderungen der Magenschleimhaut durch eine erhöhte proliferative Aktivität ihrer Zellen verursacht werden. Dies kann zu bestimmten strukturellen und funktionellen Störungen führen und geht häufig mit einer Entzündung der Magenschleimhaut einher.
Epidemiologie
In der klinischen Gastroenterologie gilt die hyperplastische Gastritis als eine relativ selten erkannte Erkrankung des Magens, die – unter den chronischen Magenerkrankungen – etwa 3,7–4,8 % der diagnostizierten Fälle ausmacht.
Dem Journal of Clinical Investigation zufolge betrifft die Riesengastritis hypertrophica sowohl Kinder als auch Erwachsene. Bei Erwachsenen entwickelt sich diese seltene Form der Magenschleimhauterkrankung zwischen dem 30. und 60. Lebensjahr, und bei Männern wird diese Erkrankung drei- bis viermal häufiger festgestellt als bei Frauen.
Aus noch ungeklärten Gründen betrifft die polypöse hyperplastische Gastritis jedoch viel häufiger die Magenschleimhaut von Frauen im Alter von 40 bis 45 Jahren.
Ursachen hyperplastische Gastritis
Wenn bei einer endoskopischen Untersuchung des Magens Bereiche mit erhöhter Mitose der Zellen der Schleimhaut, die die Magenhöhle auskleidet, festgestellt werden, können Gastroenterologen die Diagnose einer hyperplastischen Gastritis stellen.
Das wichtigste morphologische Merkmal dieser Art von Magenläsion ist die Proliferation (Hypertrophie) der Schleimhaut – aufgrund einer Zunahme drüsenförmiger Epithelzellen und einer Veränderung ihrer Anordnung sowie einer Störung der normalen gefalteten Struktur der Schleimhaut (wodurch die innere Oberfläche eines gesunden Magens nach dem Essen zunimmt). In diesem Fall wird das Auftreten dickerer, weniger beweglicher (starrer) Falten beobachtet, die eine normale Peristaltik des Magens verhindern. Und in der lockeren submukösen (submukösen) Schicht der Oberfläche verschiedener Teile des Magens, die Elastinfasern enthält, finden sich häufig hypertrophe Knoten unterschiedlicher Größe (einzeln oder mehrfach) oder polypoide Formationen.
Der Verdauungsprozess und die physiologischen Funktionen des Magens sind äußerst komplex, und die spezifischen Ursachen der hyperplastischen Gastritis werden weiterhin erforscht. Die Ätiologie hyperplastischer Prozesse im Magen über einen längeren Zeitraum hängt mit einer Reihe von Faktoren zusammen:
- Störungen des allgemeinen Stoffwechsels, die den Regenerationsprozess der Magenschleimhaut negativ beeinflussen;
- das Vorhandensein von Autoimmunerkrankungen (perniziöse Anämie);
- Infektion mit Cytomegalovirus und Aktivierung des Bakteriums Helicobacter pylori;
- Störung der neurohumoralen und parakrinen Regulierung der Produktion von Schleimsekret durch Mukozyten der Schleimhaut und der Fundusdrüsen des Magens;
- periphere Bluteosinophilie (aufgrund parasitärer Erkrankungen wie Askariasis, Anisakiasis oder lymphatischer Filariose);
- genetisch bedingte Veranlagung zur Polyposis der Fundusdrüsen des Magens und zur adenomatösen Polyposis (die durch Mutationen in den β-Catenin- und APC-Genen verursacht wird);
- autosomal-dominantes Zollinger-Ellison-Syndrom, bei dem Mutationen im Tumorsuppressorgen MEN1 auftreten;
- verschiedene angeborene Anomalien des Magens und der Differenzierung seiner Gewebe (zum Beispiel Cronkhide-Canada-Syndrom ).
Risikofaktoren
Experten nennen solche Risikofaktoren für die Entwicklung einer hyperplastischen Gastritis wie Essstörungen; Allergien gegen bestimmte Nahrungsmittel; Mangel an essentiellen Vitaminen; toxische Wirkungen von Alkohol und krebserregenden Verbindungen, schweres Nierenversagen und Hyperglykämie. Und bei der Behandlung von hyperazider Gastritis und gastroösophagealer Refluxkrankheit mit potenten Medikamenten, die die Säuresekretion hemmen (Omeprazol, Pantoprazol, Rabeprazol usw.), steigt das Risiko, das Wachstum von Polypen zu aktivieren, die in den Bereichen der Hauptdrüsen und Foveolen (Magengruben, in die die Ausführungsgänge der Drüsen münden) auftreten. Wahrscheinlich hängt diese Lokalisierung des pathologischen Prozesses damit zusammen, dass die Regeneration der Magenschleimhaut bei einer Schädigung gerade durch die Schleimhautzellen erfolgt, die die Bereiche der Magengruben bedecken.
Pathogenese
Experten assoziieren die Pathogenese der atrophisch-hyperplastischen Gastritis des Körpers und des Antrums des Magens bei längerer Anwendung der oben genannten Protonenpumpenhemmer auch mit der Möglichkeit der Entwicklung einer nodulären Hyperplasie neuroendokriner enterochromaffinähnlicher Zellen (ECLS).
In fast 40 % der Fälle verläuft die hyperplastische Gastritis bei Kindern als lymphozytäre Gastritis mit Erosion und dem Vorhandensein von T-Lymphozyteninfiltraten (CD4- und CD8-T-Zellen) in der oberen Schicht der Magenschleimhaut. Diese Pathologie tritt häufiger bei Kindern mit Glutenunverträglichkeit (Zöliakie) oder Malabsorptionssyndrom auf.
Die Pathogenese der hyperplastischen Gastritis beruht auf einer übermäßigen Anzahl von Epithelzellen der Magenschleimhaut, die Magenschleim absondern. Dies geschieht offenbar durch eine erhöhte Produktion des mitogenen Polypeptids TGF-α (Transforming Growth Factor Alpha), dessen Moleküle an epidermale Wachstumsfaktorrezeptoren (EGFR) binden, die Zellteilung der Magenschleimhaut und die Mucinproduktion stimulieren und gleichzeitig die Säuresynthese der Belegzellen hemmen.
Symptome hyperplastische Gastritis
Die Symptome einer hyperplastischen Gastritis sind unspezifisch und sehr unterschiedlich, Gastroenterologen zählen jedoch Folgendes zu den möglichen klinischen Manifestationen dieser Krankheit: Sodbrennen, Aufstoßen mit fauligem Geschmack, Plaque auf der Rückseite der Zunge, Übelkeit, vermehrte Gasbildung, Schmerzen in der Oberbauchgegend (schmerzend, drückend oder krampfhaft), Erbrechen.
Allerdings verläuft die Erkrankung oft latent und die ersten Anzeichen fast aller Formen der hyperplastischen Gastritis sind ein unangenehmes Völlegefühl im Magen, das kurz nach dem Essen auftritt (insbesondere bei fettigen und scharfen Speisen und erhöhtem Säuregehalt des Magensaftes).
Bei einer erosiv-hyperplastischen Gastritis klagen Patienten über Magenschmerzen, die beim Gehen oder Beugen des Körpers stärker werden können. Bei manchen kommt es im Frühjahr zu einer Verschlimmerung der Krankheit mit dem Auftreten von Blut im Stuhl (Meläna). Auch im Erbrochenen kann Blut enthalten sein.
In den meisten Fällen einer hypertrophen Riesengastritis treten keine Symptome auf. Bei manchen Patienten können jedoch Schmerzen in der Magengrube, Übelkeit mit Erbrechen und Durchfall auftreten. Außerdem treten Appetitlosigkeit und Gewichtsverlust, Hypoalbuminämie (niedriger Albumingehalt im Blutplasma) und eine damit verbundene Schwellung des Magengewebes auf. Auch Magenblutungen sind möglich.
Formen
Derzeit gibt es keine einheitliche Klassifikation der hyperplastischen Gastritis, Gastroenterologen verwenden jedoch das sogenannte Sydney-Klassifikationssystem für Gastritis (das von den Teilnehmern des 9. Weltkongresses für Gastroenterologie übernommen wurde).
Experten betonen, dass es sich – unabhängig von Lokalisation, Schweregrad und Stadium (Exazerbation oder Remission) – um eine chronische hyperplastische Gastritis handelt. In der häuslichen Gastroenterologie werden folgende Arten dieser Pathologie unterschieden:
- Fokale hyperplastische Gastritis oder noduläre endokrine Zellhyperplasie ist die Entwicklung eines basal gelegenen gutartigen Magenkarzinoidtumors (<1-1,5 cm groß), der als Folge einer Hyperplasie endokriner enterochromaffiner Zellen auftritt, deren Proliferation durch Hypergastrinämie (Überschuss des Hormons Gastrin) stimuliert wird. Am häufigsten wird diese Pathologie bei Patienten mit chronischer atrophischer Gastritis, Vitamin-B12-Mangel (perniziöse Anämie) sowie mit Mutationen des MEN1-Tumorsuppressorgens (was zu multipler endokriner Neoplasie führt) beobachtet.
- Eine diffuse hyperplastische Gastritis wird diagnostiziert, wenn hypertrophe Veränderungen der Magenschleimhaut jeglicher Ätiologie vielfältiger Natur sind.
- Die oberflächliche hyperplastische Gastritis ist dadurch gekennzeichnet, dass nur das obere einschichtige prismatische Epithel der Magenschleimhaut am pathologischen Prozess beteiligt ist.
- Polypöse hyperplastische Gastritis, die viele Spezialisten als atrophisch-hyperplastisch definieren und offiziell als multifokale atrophische Gastritis mit fokaler Hyperplasie bezeichnet wird. Das Auftreten multipler Polypen, bestehend aus Drüsengewebezellen auf der Schleimhaut der Magenwände, ist mit einer Helicobacter-pylori-Infektion sowie mit Hypochlorhydrie und Hypergastrinämie der Autoimmunätiologie verbunden. In der Regel beginnt sich die Pathologie im Erwachsenenalter zu manifestieren; sie hat sowohl fokale als auch diffuse Formen.
- Erosiv-hyperplastische Gastritis oder lymphozytär-erosive Gastritis (die bereits oben erwähnt wurde) ist nicht nur durch Leukozyteninfiltrate in der Magenschleimhaut und Hypertrophie ihrer Falten gekennzeichnet. Es können auch knotige Formationen und Bereiche chronischer Erosion der Schleimhaut (insbesondere im Bereich der Foveolae der Herz-, Fundus- und Pylorusdrüsen) beobachtet werden. In diesem Fall kann der Säuregehalt des Magensaftes unterschiedlich sein.
- Hyperplastische granuläre Gastritis (oder granuläre) wird als fokale Hypertrophie der Schleimhaut klassifiziert, wenn sich darauf mehrere 1-3 mm große halbkugelförmige Wucherungen bilden, die dazu führen, dass die Schleimhaut anschwillt und knotig wird. Gleichzeitig wird eine Starrheit der Muskelplatte, der Submukosa sowie der Falten der Schleim- und Muskelmembran des Magens festgestellt. Die typische Lokalisation ist der Antrumabschnitt, dessen Schleimhaut eine große Anzahl zusätzlicher sekretorischer Zellen mit granulärem Zytoplasma und Einschluss von Schleimgranula aufweist, die Schleimsekret produzieren. Klinischen Beobachtungen zufolge wird diese Pathologie häufiger bei Männern mittleren Alters festgestellt.
- Bei der hyperplastischen Refluxgastritis kommt es zum Rückfluss von Zwölffingerdarminhalt in den Magen, wodurch das Schleimhautepithel des Magens durch Bestandteile des Zwölffingerdarmsekrets (vor allem Gallensäuren) geschädigt wird.
- Antrale hyperplastische Gastritis oder rigide antrale Gastritis manifestiert sich in der Störung des physiologisch normalen Reliefs der Schleimhaut, bis hin zu einer Veränderung der Faltenrichtung, sowie im Vorhandensein von polypösen Formationen auf ihrer Oberfläche. Aus diesem Grund können die Haupt- und Belegzellen der Fundusdrüsen verkümmern, was zu Achlorhydrie (Einstellung der Salzsäureproduktion) führt. Darüber hinaus wird der Pylorusteil des Magens deformiert und verengt sich, und die Magenperistaltik nimmt ab.
Zu den seltenen Erbkrankheiten zählt die gigantische hypertrophe Gastritis – die chronische hypertrophe polyadenomatöse Gastritis oder Morbus Menetrier. Sie ist gekennzeichnet durch eine Hypertrophie der Schleimhaut in den Magengruben und eine deutliche Zunahme der Magenfalten, eine unzureichende Salzsäuresekretion und eine übermäßige Produktion von schützendem Magenschleim. Niedrige Salzsäurespiegel führen zur Unfähigkeit, Proteine zu verdauen und Nährstoffe aufzunehmen, was zu Durchfall, Gewichtsverlust und peripheren Weichteilödemen führt. Da die Entzündung jedoch minimal ist oder fehlt, wird der Morbus Menetrier in der medizinischen Literatur als eine Form der hyperplastischen Gastropathie eingestuft.
Schließlich gibt es noch die aktive hyperplastische Gastritis, die eine dreistufige leukozytäre (neutrophile) Infiltration von Schleimhauthyperplasieherden aufweist. Im Wesentlichen handelt es sich dabei um eine chronische hyperplastische Gastritis, bei der der Schweregrad des Entzündungsprozesses, der durch histologische Untersuchung von Gewebeproben bestimmt wird, in Abhängigkeit vom Ausmaß des Eindringens polynukleärer T-Zellen in die Strukturen der Magenschleimhaut eingestuft wird.
Komplikationen und Konsequenzen
Die häufigsten Folgen und Komplikationen einer hyperplastischen Gastritis:
- Veränderungen in der Struktur der Magenschleimhaut mit Atrophie unterschiedlichen Schweregrades;
- Schädigung und Verringerung der Anzahl der Belegzellen, verminderte Säuresynthese und Verschlechterung der Verdauungsfunktionen des Magens;
- Atonie und beeinträchtigte Magenmotilität, was zu anhaltender Dyspepsie und teilweiser Gastroparese führt;
- Hypoproteinämie (Abnahme des Serumproteinspiegels);
- Anämie;
- Gewichtsverlust.
Eine fortgeschrittene hyperplastische granuläre Gastritis bedroht die Entwicklung von Magengeschwüren und sogar Krebs. Eine riesige hypertrophe Gastritis führt zu Hypochlorhydrie; Experten weisen darauf hin, dass diese Form der Pathologie zu einem krebsartigen Tumor des Magens degenerieren kann.
Eine fokale Hyperplasie enterochromaffinähnlicher Zellen der Schleimhaut kann auch zu Magenkarzinomen führen. Eine polypöse hyperplastische Gastritis entwickelt sich einigen Daten zufolge in fast 20 von 100 Fällen bösartig.
Diagnose hyperplastische Gastritis
Die Hauptmethode zur Diagnose einer hyperplastischen Gastritis ist die Endogastroskopie (Endogastroduodenoskopie). Die endoskopische instrumentelle Diagnostik ermöglicht nicht nur die Visualisierung pathologisch veränderter Bereiche der Magenschleimhaut, sondern auch die Durchführung einer Biopsie: die Entnahme von Gewebepartikeln zur anschließenden histochemischen Untersuchung. Röntgen, Ultraschall des Magens und Elektrogastrographie werden ebenfalls eingesetzt.
Es werden Laboruntersuchungen durchgeführt, bei denen folgende Analysen durchgeführt werden:
- klinische und biochemische Blutanalyse;
- Bluttest auf Eosinophile;
- IF-Bluttest auf das Vorhandensein von Helicobacter pylori;
- Magensaft zur Bestimmung des pH-Werts;
- Bluttest auf Magenkrebs-Tumormarker CA72-4;
- Stuhlanalyse.
Was muss untersucht werden?
Welche Tests werden benötigt?
Differenzialdiagnose
Um alle genannten Formen der Magenschleimhauthyperplasie von anderen Gastritiden, gastroduodenalen Erkrankungen und Magen-Onkopathologien abzugrenzen, wird eine Differentialdiagnose durchgeführt.
Wen kann ich kontaktieren?
Behandlung hyperplastische Gastritis
Heute wird eine symptomatische Behandlung der hyperplastischen Gastritis durchgeführt, die die Ätiologie der Krankheit, ihre Art und ihre Hauptmanifestationen berücksichtigt. Und natürlich der Säuregehalt des Magensaftes.
Bei einem positiven H. pylori-Test wird eine Eradikationskur verordnet, die das Azalid-Antibiotikum Azithromycin (Sumamed) – drei Tage, zwei Kapseln (1 g) – sowie das antibakterielle Medikament der Makrolidgruppe Clarithromycin (Aziclar, Claricin) – 14 Tage lang, 500 mg zweimal täglich – umfasst. Zu den Nebenwirkungen dieser Medikamente zählen Magen-, Gallenblasen- und Darmprobleme, Kopfschmerzen, Tachykardie, Parästhesien usw.
Bei einem pH-Wert <5–6 sind Medikamente zur Verringerung der Säuresekretion erforderlich: Ranitidin-Tabletten (0,3 g einmal täglich); Quamatel (20 mg zweimal täglich); Misoprostol (Cytotec) – eine Tablette dreimal täglich.
Präparate mit Wismutsubcitrat (Ventrisol, Bismofal, De-Nol Sucralf usw.) sowie Aluminiumverbindungen (Gelusil, Compensan, Gastal usw.) schützen die geschädigte Schleimhaut vor den Auswirkungen der Magensäure. Bruscopan und Pirenzepin (Gastrocepin, Gastril, Riabal) lindern Schmerzen. Weitere Informationen zu Dosierung, Kontraindikationen und Nebenwirkungen dieser Medikamente finden Sie in den Artikeln „Tabletten gegen Magengeschwüre“ und „ Tabletten gegen Bauchschmerzen“.
Bei Schleimhautatrophie empfehlen Ärzte die Einnahme von Vitamin P und B-Vitaminen, insbesondere Cyanocobalamin (B12). Methionin kann zur Korrektur des mit Hypoproteinämie verbundenen Zustands eingesetzt werden (0,5–1,5 g dreimal täglich für zwei bis drei Wochen).
Für diese Pathologie bietet die Homöopathie ein Mehrkomponentenmittel zur parenteralen und inneren Anwendung (täglich oder jeden zweiten Tag) an – eine Lösung in Ampullen von Mucosa compositum.
Eine chirurgische Behandlung kann bei schwerer fokaler und polypöser hyperplastischer Gastritis sowie bei periodischen Magenblutungen durchgeführt werden.
Und wie die physiotherapeutische Behandlung durchgeführt wird, wird in der Veröffentlichung ausführlich beschrieben - Physiotherapie bei chronischer Gastritis
Eine Diät bei hyperplastischer Gastritis des Magens hat ein großes therapeutisches Potenzial – wie bei den meisten Erkrankungen des Verdauungssystems, lesen Sie den Artikel – Diät bei Gastritis
Hausmittel
Die traditionelle Behandlung der hyperplastischen Gastritis umfasst eine Kräuterbehandlung in Form von Abkochungen und Wasseraufgüssen, die im Verhältnis von einem Esslöffel Pflanzenmaterial auf 200–250 ml Wasser zubereitet werden.
Am häufigsten wird in der Kräutermedizin die Verwendung von Kamille (Blüten), Wegerich (Blätter), Ringelblume (Blüten), Fingerkraut und Thymian (Kraut) empfohlen.
Ein Sud aus den Wurzeln von Orchis bifolia und Blutweiderich wirkt als Umhüllungsmittel (dreimal täglich 50–60 ml). Und ein Aufguss aus Weidenröschen (Weidenröschen), viermal täglich einen Esslöffel, hilft bei Entzündungen der Magenschleimhaut.
Weitere Informationen zur Behandlung
Verhütung
Zur Vorbeugung gehört vorerst nur die Reihenfolge und Regelmäßigkeit der Ernährung, die fünfmal täglich erfolgen sollte und etwas mehr Proteinprodukte enthalten sollte. Wichtig ist eine ausreichende Menge an Vitaminen (aber in Gemüse und Obst ohne grobe Ballaststoffe) und Wasser (mindestens fünf Gläser pro Tag).


 [
[