Facharzt des Artikels
Neue Veröffentlichungen
Medikamente
Dopamin
Zuletzt überprüft: 03.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Dopamin (DA) ist ein peripherer Vasodilatator, der zur Behandlung von niedrigem Blutdruck, niedriger Herzfrequenz und Herzstillstand, insbesondere in der Neugeborenen-Akutversorgung, durch kontinuierliche intravenöse Infusion eingesetzt wird. [ 1 ] Niedrige Infusionsraten (0,5 bis 2 µg/kg pro Minute) wirken auf die Splanchnikusgefäße und führen zu einer Gefäßerweiterung, einschließlich der Nieren, was zu einer erhöhten Urinausscheidung führt. Mittlere Infusionsraten (2 bis 10 µg/kg/min) stimulieren die myokardiale Kontraktilität und erhöhen die elektrische Reizleitung im Herzen, was zu einem erhöhten Herzzeitvolumen führt. Höhere Dosen verursachen über die adrenergen α-1-, β-1- und β-2-Rezeptoren eine Gefäßverengung und einen erhöhten Blutdruck, was möglicherweise zu einem peripheren Kreislaufkollaps führt. [ 2 ]
Hinweise Dopamin
Indikationen für den Einsatz von Dopamin umfassen die Aufrechterhaltung des Blutdrucks bei chronischer Herzinsuffizienz, Trauma, Nierenversagen und sogar Operationen am offenen Herzen sowie Schock durch Herzinfarkt oder Sepsis. Die Verabreichung von niedrig dosiertem DA kann auch zur Behandlung von Hypotonie, niedrigem Herzzeitvolumen und Organversagen (oft erkennbar an einer geringen Urinausscheidung) nützlich sein. DA erlangte erhebliche klinische Bedeutung im zentralen Nervensystem (ZNS), nachdem Horniewicz’ Experimente seine Verringerung des Nucleus caudatus bei Patienten mit Parkinson-Krankheit zeigten. Darüber hinaus schwächt die intravenöse Verabreichung seines Aminosäurevorläufers L-DOPA (L-Dihydroxyphenylalanin) die Parkinson-Symptome ab.[ 3 ] Da die Blut-Hirn-Schranke verhindert, dass DA aus dem systemischen Kreislauf in das ZNS gelangt, ist DA bei zentralen neurologischen Erkrankungen wie der Parkinson-Krankheit wirkungslos. L-DOPA passiert jedoch erfolgreich die Blut-Hirn-Schranke und kann systemisch verabreicht werden, auch in Form von Tabletten. Obwohl eine therapeutische Dopaminsubstitution die motorischen Symptome wirksam lindert, kann sie zu motorischen Nebenwirkungen und suchtbedingten Verhaltensproblemen (z. B. Impulskontrollstörungen) führen [ 4 ], [ 5 ], [ 6 ].
Freigabe Formular
Dopamin ist in Ampullen als Konzentrat zur Herstellung einer Infusionslösung erhältlich.
Pharmakodynamik
Die Dopaminbiosynthese folgt der gleichen enzymatischen Sequenz wie die von Noradrenalin (NE). Tatsächlich ist DA eine Vorstufe der NE-Synthese (siehe Abbildung). [ 7 ], [ 8 ] Der erste Schritt der DA-Synthese ist geschwindigkeitsbestimmend und beinhaltet die Umwandlung von L-Tyrosin in L-DOPA durch das Enzym Tyrosinhydroxylase (TH). [ 9 ], [ 10 ] Diese Umwandlung benötigt Sauerstoff, einen Eisen-Cofaktor und Tetrahydrobiopterin (BH4 oder THB) und führt zur Addition einer Hydroxygruppe an den aromatischen Ring unter Bildung von L-DOPA. Dieses Molekül wird anschließend durch aromatische L-Aminosäure-Decarboxylase unter Entfernung der Carboxylgruppe in DA umgewandelt. Nach der Synthese wird DA über den vesikulären Monoamintransporter 2 (VMAT2) in synaptische Vesikel zu den synaptischen Enden transportiert. [ 11 ], [ 12 ]
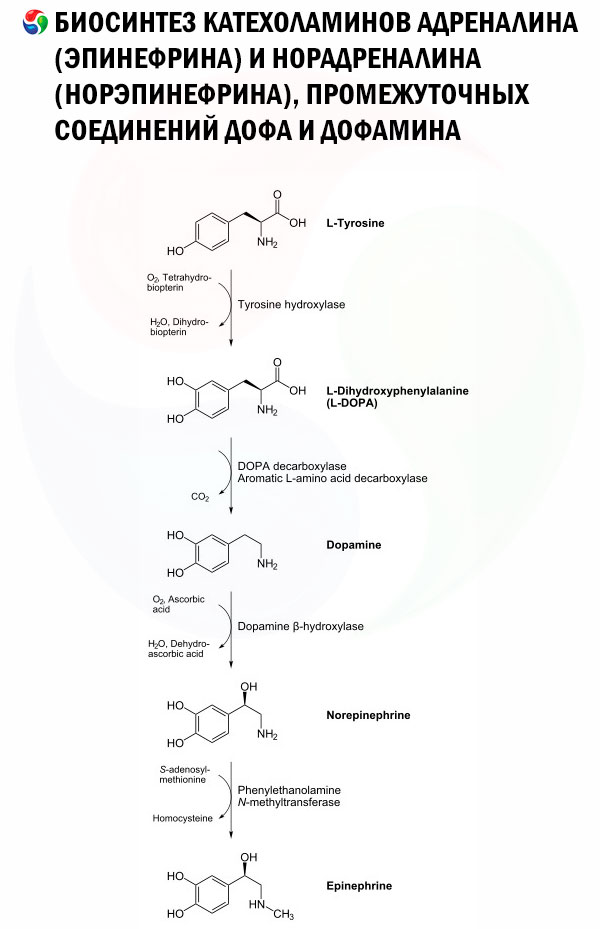
Bei regelmäßiger Einnahme großer Mengen von L-Tyrosin passiert es, genau wie L-DOPA, problemlos die Blut-Hirn-Schranke. [ 13 ] Sein Nutzen ist jedoch räumlich begrenzt, da DA die Blut-Hirn-Schranke nicht überwinden kann. Bei niedrigem L-Tyrosinspiegel kann L-Phenylalanin jedoch durch die Phenylalaninhydroxylase in L-Tyrosin umgewandelt werden.
Sobald DA in den synaptischen Raum freigesetzt wird, interagiert es mit verschiedenen Rezeptoren an den prä- und postsynaptischen Endigungen und verursacht so die Erregung oder Hemmung von Zielneuronen. Es gibt zwei ganze Familien von DA-Rezeptoren, bestehend aus fünf verschiedenen Isoformen, von denen jede unterschiedliche intrazelluläre Signalwege beeinflusst.[ 14 ] Beide Familien von Dopaminrezeptoren, D1 und D2, sind per Definition G-Protein-gekoppelte Rezeptoren, wobei die Rezeptorklasse D1 zu neuronaler Depolarisation führt, während D2-Rezeptoren die neuronale Erregung unterdrücken.[ 15 ]
Im synaptischen Spalt angekommen, wird DA über DA-Transporter (DATs) zur Neuverpackung zurück in das präsynaptische Neuron transportiert oder verbleibt im extrazellulären Raum, wo es von Gliazellen aufgenommen oder durch die Zellmembran verstoffwechselt wird. DA kann extraneuronal durch Catechol-O-Methyltransferase (COMT) zu 3-Methoxytyramin (3-MT) metabolisiert werden, während Monoaminooxidase-B (MAO-B) 3-MT schnell zu Homovanillinsäure (HVA) verstoffwechselt.[ 16 ] Darüber hinaus kann es im Zytoplasma verstoffwechselt werden, wo die Doppelwirkung von MAO-A und Aldehyddehydrogenase (ALDH) DA in die Phenolsäure 3,4-Dihydroxyphenylessigsäure (DOPAC) umwandelt.[ 17 ]
Aufgrund dieser komplexen Abfolge kann die Dopaminmodulation auf verschiedenen Ebenen erfolgen, beispielsweise im gesamten Neuron, seinen Projektionen oder neuronalen Schaltkreisen des Nervensystems. Darüber hinaus kann sie während der DA-Synthese (transkriptionelle, translationale und posttranslationale Regulation), der synaptosomalen Verpackung (VMAT-Regulation, Vesikeltransport in die Synapse), der DA-Freisetzung (neuronale Depolarisation, Kalziumsignalisierung, Vesikelfusion) sowie durch Wiederaufnahme und Metabolismus durch die Regulierung der entsprechenden Enzyme und ihrer räumlichen Lokalisierung relativ zu ihrem Substrat erfolgen. [ 18 ]
Wie bereits erwähnt, hängt die systemische Wirkung von DA von verschiedenen Rezeptoren (D1, D2, D3, D4 und D5) sowie alpha- und beta-adrenergen Rezeptoren ab. Diese G-gekoppelten Rezeptoren werden üblicherweise als D1 oder D2 gruppiert, hauptsächlich aufgrund ihrer traditionellen biochemischen Funktionen, die darauf hindeuten, dass Dopamin die Adenylatcyclase-Aktivität modulieren kann.[ 19 ] Aufgrund ihrer molekularen Struktur, biochemischen Eigenschaften und pharmakologischen Funktionen werden DA-Rezeptoren jedoch weiter in die Klassen D1 (D1 und D5) und D2 (D2, D3, D4) eingeteilt.[ 20 ],[ 21 ]
Die Aktivierung von D1-Rezeptoren an der glatten Muskulatur, dem proximalen Nierentubulus und dem kortikalen Sammelrohr erhöht die Diurese.[ 22 ] D2-Rezeptoren befinden sich präsynaptisch an den Nierennerven, Glomeruli und der Nebennierenrinde. Die Aktivierung dieser Nerven führt zu einer verminderten renalen Natrium- und Wasserausscheidung.[ 23 ] Apomorphin ist ein DA-Rezeptoragonist und könnte eine ähnliche Aktivierung an diesen DA-Rezeptoren bewirken.[ 24 ] Adrenerge Rezeptoren binden ebenfalls DA, wodurch die Kontraktion der arteriellen glatten Muskulatur und die Reizleitung im Sinusknoten des Herzens erhöht werden, was seinen therapeutischen Nutzen für das Herz erklärt.
Obwohl die Blut-Hirn-Schranke den DA-Transfer vom systemischen Kreislauf zum zentralen Nervensystem spezifisch begrenzt, führten weitere Forschungen zur Entdeckung seiner zentralen Rolle im Belohnungsverhalten, bei dem sein Transfer deutlich erhöht ist. Aktuelle Forschungen zu DA umfassen epigenetische Veränderungen und deren Beteiligung an verschiedenen psychiatrischen Erkrankungen, darunter Substanzmissbrauch und Sucht, Schizophrenie und Aufmerksamkeitsdefizitstörung.[ 25 ],[ 26 ] Im Allgemeinen gehen diese Erkrankungen mit Störungen der mesolimbischen und mesokortikalen DA-Bahnen einher. Eine häufige Wirkung von Suchtmitteln im ZNS ist eine erhöhte DA-Freisetzung im Striatum, die typischerweise mit hoher Bewegungsaktivität und Stereotypie einhergeht. [ 27 ] Die Zunahme der DA im Striatum ist das Ergebnis axonaler Projektionen, die direkt aus der Substantia nigra pars compacta (SN) bzw. dem ventralen tegmentalen Areal (VTA) entspringen und in den Nucleus accumbens und die Amygdala projizieren.[ 28 ],[ 29 ]
Ein weiterer DA-Schaltkreis, der tuberoinfundibuläre Pfad, ist hauptsächlich für die Regulierung des neuroendokrinen Prolaktins aus dem Hypophysenvorderlappen verantwortlich und ist bekannt für seine Rolle als Induktor der Laktation, spielt aber auch eine untergeordnete Rolle bei der Wasser-Salz-Homöostase, der Immunantwort und der Zellzyklusregulation.[ 30 ],[ 31 ] Der nigrostriatale Pfad ist der wichtigste Pfad, der an den motorischen Defiziten bei der Parkinson-Krankheit beteiligt ist.[ 32 ] An diesem Pfad sind dopaminerge Neuronen beteiligt, die in der Substantia nigra (Pars compacta) entstehen und über das mediale Vorderhirnbündel zum Striatum projizieren, wo sie Synapsen mit mehreren neuronalen Populationen im Putamen, Nucleus caudatus, Globus pallidus interna (GPi) und Nucleus subthalamicus (STN) bilden. Dieses komplexe Netzwerk bildet afferente Verbindungen von der Substantia nigra zu dem an der motorischen Bewegung beteiligten Schaltkreis, nämlich den Basalganglien. Bei letzterem spielt DA eine Schlüsselrolle bei der Kontrolle motorischer Bewegungen und dem Erlernen neuer motorischer Fähigkeiten. [ 33 ]
Dosierung und Verabreichung
Zur Stimulation des sympathischen Nervensystems ist eine kontinuierliche intravenöse Tropfinfusion angezeigt. Die Halbwertszeit von Dopamin im systemischen Kreislauf beträgt 1 bis 5 Minuten; daher sind langsamere Verabreichungsformen, wie die orale Verabreichung, in der Regel unwirksam.[ 38 ]
Neben seinen peripheren sympathischen Wirkungen ist DA auch für die neurologische Motorik bei Parkinson entscheidend. L-DOPA wird oral verabreicht, und nach der Resorption gelangt ein geringer Anteil ins Gehirn, wo es von Neuronen in den Basalganglien verarbeitet wird. L-DOPA wird üblicherweise zusammen mit Carbidopa verabreicht, um die peripheren Effekte von L-DOPA auf das sympathische Nervensystem zu hemmen. Carbidopa ist ein Decarboxylasehemmer, der die systemische Umwandlung von L-DOPA in DA verhindert und so häufige Nebenwirkungen wie Übelkeit und Erbrechen reduziert.[ 39 ]
Kontraindikationen
Intravenöses Dopamin ist bei Patienten mit Herz- oder Kreislauferkrankungen kontraindiziert. Zu diesen Erkrankungen können ventrikuläre Arrhythmien und Tachykardie, Gefäßverschluss, niedriger Blutsauerstoffgehalt, verringertes Blutvolumen, Azidose und Nebennierenfunktionsstörungen mit daraus resultierendem Bluthochdruck, wie z. B. Phäochromozytom, gehören. Bei Patienten, die kürzlich mit Monoaminooxidasehemmern behandelt wurden, sollte DA anfänglich in fraktionierten Dosen (einem Zehntel der üblichen Dosis) verabreicht und weitere Wirkungen genau überwacht werden. Medikamente zur Behandlung von Bluthochdruck, wie z. B. Beta- und Alpha-Adrenozeptorhemmer, wirken den therapeutischen Wirkungen von DA entgegen. Haloperidol blockiert außerdem die systemischen Wirkungen von DA. Es wurde berichtet, dass das Antikonvulsivum Phenytoin in Kombination mit DA Hypotonie und Herzfrequenz verursacht. Andererseits verstärken trizyklische Antidepressiva die DA-Reaktion, ähnlich wie Anästhetika wie Cyclopropan und halogenierte. In Kombination mit Oxytocin kann die Einnahme von DA zu chronischer Hypertonie führen und auch zerebrovaskuläre Unfälle verursachen.[ 34 ]
Nebenwirkungen Dopamin
Die Verabreichung von Dopamin kann die Nierenfunktion beeinträchtigen und zu vermehrtem Wasserlassen und unregelmäßigem Herzschlag führen.[ 35 ] Eine übermäßige Verabreichung kann aufgrund des erhöhten Blutdrucks im Gehirn gefährliche Zustände wie zerebrovaskuläre Unfälle verursachen.[ 36 ]
Wie bereits erwähnt, wirkt der Neurotransmitter DA auch im zentralen mesokortikolimbischen Pfad und spielt eine Rolle bei der Belohnungs- und Angstverarbeitung sowie bei der Aufmerksamkeitsfokussierung und exekutiven Funktionen, einschließlich komplexer Planung. Während systemisches Dopamin die Blut-Hirn-Schranke nicht passiert, wird zentrales Dopamin mit Schläfrigkeit, Schizophrenie, Sucht und Impulskontrollstörungen in Verbindung gebracht.[ 37 ] Patienten mit neurologischen Erkrankungen, die hohe Dosen von L-DOPA zur Behandlung der Parkinson-Krankheit einnehmen, können aufgrund einer Dysregulation von DA in den ZNS-Bahnen solche physiologischen Veränderungen erfahren.
Lagerbedingungen
An einem lichtgeschützten Ort.
Spezielle Anweisungen
Die Überwachung von Blutdruck und Harnfluss ist notwendig. Ebenso wird eine Überwachung komplexerer hämodynamischer Parameter wie Herzzeitvolumen einschließlich Rhythmus und pulmonalarteriellem Verschlussdruck empfohlen. Es ist erwähnenswert, dass Dopaminagonisten und -mimetika, die die Blut-Hirn-Schranke durchdringen, mit neurologischen Schaltkreisen interagieren, die an motorischen, exekutiven und limbischen Funktionen beteiligt sind, darunter suchtbezogene Belohnungssysteme, Impulskontrollmechanismen und Erregung. Daher kann das Absetzen einer DA-Therapie zu einem sogenannten Dopaminagonisten-Entzugssyndrom führen. Dieser Zustand hat ein breites Spektrum an Symptomen, darunter Angstzustände, Depressionen, Panikattacken, Müdigkeit, Hypotonie, Übelkeit, Reizbarkeit und sogar Suizidgedanken. [ 43 ] Patienten wird daher geraten, diese zentral wirkenden DA-Agonisten schrittweise abzusetzen.
Haltbarkeit
Die Haltbarkeit beträgt 2 Jahre.
Dopaminmangel
Zahlreiche Studien untersuchen die Rolle von Dopamin bei der Beteiligung an Bewegungen und sensorischen und motorischen Funktionen. Demnach treten bei einem Dopaminmangel in dopaminergen Endigungen ohne pharmakologische Intervention oder Gentherapie und damit bei DA-Mangel Defekte in vielen dieser Funktionen auf. [ 44 ]
Überschüssiges Dopamin
In diesem Fall müssen wir ein solches Phänomen anhand eines Beispiels betrachten. Jemand beginnt eine Diät und ist fest entschlossen, das Begonnene zu Ende zu bringen. Doch dann kommt ein leckerer Kuchen und alles ist vorbei. Dadurch verliert der Mensch die Kontrolle über sich selbst. Er braucht eine Dosis des „Glückshormons“, und genau diese süße Freude kann es auslösen. Wenn man also einen Kuchen isst, dann den zweiten, kann man einfach nicht aufhören. Dadurch entsteht genau dieser Dopaminüberschuss. Daran ist nichts Schlimmes. Aber es ist ziemlich schwierig für einen Menschen, damit aufzuhören.
Letztendlich ist es durch die Abhängigkeit von einem weiteren „Lebenssüßstoff“ schlicht unmöglich, die Kontrolle auszuüben. Ein Mensch ist dazu nicht mehr in der Lage. Er macht einfach weiter und wird dadurch dick oder verschlechtert seine Gesundheit. Alles hängt davon ab, welche Rolle dieses Glückshormon spielt.
Dopamin kann viele Aspekte bewusster Aktivität beeinflussen. Es ist notwendig, seinen Spiegel zu senken und einen Überschuss zu vermeiden. Dies kann aber auch „gefährlich“ sein, da eine Verringerung der Impulsivität zu Schäden an anderen, ebenso wichtigen Funktionen führen kann.
Dopamin-Wiederaufnahmehemmer
Dopamin-Wiederaufnahmehemmer (DRIs) sind eine Klasse von Medikamenten, die als Wiederaufnahmehemmer des monoaminergen Neurotransmitters Dopamin wirken, indem sie die Wirkung des Dopamintransporters (DAT) blockieren. Die Wiederaufnahmehemmung wird erreicht, indem extrazelluläres Dopamin, das nicht vom postsynaptischen Neuron aufgenommen wird, daran gehindert wird, wieder in das präsynaptische Neuron einzudringen. Dies führt zu erhöhten extrazellulären Dopaminkonzentrationen und einer erhöhten dopaminergen Neurotransmission.[ 48 ]
Dopamin-Wiederaufnahmehemmer werden aufgrund ihrer psychostimulierenden Wirkung zur Behandlung von Aufmerksamkeitsdefizit-/Hyperaktivitätsstörungen (ADHS) und Narkolepsie sowie aufgrund ihrer appetitzügelnden Wirkung zur Behandlung von Fettleibigkeit und Essattacken eingesetzt. Sie werden gelegentlich auch als Antidepressiva zur Behandlung von Stimmungsstörungen eingesetzt, ihr Einsatz als Antidepressiva ist jedoch aufgrund des hohen Missbrauchspotenzials potenter DRIs und gesetzlicher Einschränkungen ihrer Anwendung begrenzt. Eine fehlende Dopamin-Wiederaufnahme und erhöhte extrazelluläre Dopaminspiegel werden mit einer erhöhten Anfälligkeit für Suchtverhalten in Verbindung gebracht, wenn die dopaminerge Neurotransmission erhöht ist. Es wird angenommen, dass der dopaminerge Signalweg in Belohnungszentren eine starke Rolle spielt. Viele DRIs, wie z. B. Kokain, sind aufgrund der belohnenden Wirkung, die durch erhöhte synaptische Dopaminkonzentrationen im Gehirn hervorgerufen wird, missbrauchsgefährdet.
Die folgenden Arzneimittel weisen DRI-Aktivität auf und wurden bzw. werden klinisch speziell aufgrund dieser Eigenschaft eingesetzt: Amineptin, Dexmethylphenidat, Diphemetorex, Fencamfamin, Lefetamin, Levofacetophenon, Medifoxamin, Mesocarb, Methylphenidat, Nomifensin, Pipradrol, Prolintan und Pyrovaleron. Die folgenden Arzneimittel werden bzw. wurden klinisch eingesetzt und weisen nur eine schwache DRI-Aktivität auf, die klinisch relevant sein kann, jedoch nicht muss: Adrafinil, Armodafinil, Bupropion, Mazindol, Modafinil, Nefazodon, Sertralin und Sibutramin.
Dopaminblocker
Die Ausprägung vieler unkonditionierter und konditionierter Verhaltensweisen kann durch D1- und D2-Antagonisten beeinträchtigt werden. Beispielsweise reduzieren D1- und D2-Antagonisten die Bewegungsaktivität [ 49 ], [ 50 ], [ 51 ] und die Häufigkeit appetitmotivierten operanten Verhaltens. [ 52 ], [ 53 ], [ 54 ], [ 55 ] Allerdings scheint zumindest ein Aspekt der Verhaltensausprägung, die Dauer von Verhaltenshandlungen, durch D2-Rezeptorantagonisten (im Vergleich zu D1) relativ spezifisch moduliert zu werden.
Wir haben bereits früher beobachtet, dass eine systemische Blockade des D1-Rezeptors den Anteil der Versuche verringert, in denen der konditionierte Reiz (CS) eine Annäherungsreaktion hervorruft. Dieser Effekt wurde nach einer Blockade des D2-Rezeptors nicht beobachtet.[ 56 ] Andere Studien berichteten ebenfalls von einer Beeinträchtigung der Expression von Reizreaktionen durch die Blockade des D1-,[ 57 ] aber nicht durch die Blockade des D2-,[ 58 ],[ 59 ]-Rezeptors, obwohl in mehreren Studien eine Beeinträchtigung der Expression von Reizreaktionen durch D2-Antagonisten beobachtet wurde.[ 60 ],[ 61 ]
Dopaminaustausch
Wissen Sie, wie Dopamin ausgetauscht wird? Heutzutage wird aktiv nach Wirkstoffen mit dopaminerger Wirkung gesucht. Ein chronischer Mangel kann zu verschiedenen Veränderungen der Rezeptorfunktion führen.
Eine Langzeitbehandlung kann zu irreversiblen Veränderungen der dopaminergen Rezeptoren führen. Dies stoppt jedoch nicht die fortschreitende Degeneration des präsynaptischen Neurons. Deshalb wurde nach speziellen Mitteln gesucht, die postsynaptische Rezeptoren stimulieren und sie therapieempfindlicher machen können. Dazu gehören dopaminerge Agonisten. Es gibt jedoch auch Bedenken. So kann die langfristige Anwendung dopaminerger Agonisten zu einer Hemmung der Tyrosinhydroxylase-Aktivität führen.
 [ 62 ], [ 63 ], [ 64 ], [ 65 ], [ 66 ], [ 67 ]
[ 62 ], [ 63 ], [ 64 ], [ 65 ], [ 66 ], [ 67 ]
Dopaminproduktion
Wissenschaftler haben bewiesen, dass jede Aktivität, die Freude bereitet, zur Produktion des Glückshormons führt. Daher ist es völlig egal, was jemand tut, Hauptsache, es macht ihn glücklich. Natürlich sollten die Aktivitäten in vernünftigen Grenzen bleiben. Wenn man alle Freuden ausschließt, sinkt der Dopaminspiegel deutlich und man kann in eine Depression verfallen.
Man muss verstehen, dass Dopamin mit einer Art Drogenabhängigkeit in Verbindung gebracht wird. Denn wer Kuchen liebt, isst ihn ständig, um seine Stimmung zu verbessern. Das führt zu weiteren Problemen wie schlechter Gesundheit, Übergewicht usw. Nimmt man die „Freude“, treten Depressionen auf und die Stimmung verschlechtert sich. Letztendlich ist es ein Teufelskreis. Daher müssen Sie sich sinnvollere Aktivitäten suchen.
Der einfachste und angenehmste Weg, die „Produktion“ von Dopamin auszulösen, ist regelmäßiger Sex. Nur wenn diese Aktivität wirklich Freude bereitet.
 [ 68 ], [ 69 ], [ 70 ], [ 71 ]
[ 68 ], [ 69 ], [ 70 ], [ 71 ]
Dopamin und Schizophrenie
Die Ursprünge der Dopamin-Hypothese liegen in zwei Beweislinien. Erstens zeigten klinische Studien, dass dopaminerge Agonisten und Stimulanzien bei gesunden Personen Psychosen auslösen und bei Patienten mit Schizophrenie diese verschlimmern können.[ 72 ] Zweitens wurde festgestellt, dass Antipsychotika das Dopaminsystem beeinflussen.[ 73 ] Später wurde die Wirksamkeit von Antipsychotika mit ihrer Affinität zu Dopamin-D2-Rezeptoren in Verbindung gebracht, wodurch die molekulare Wirkung mit dem klinischen Phänotyp verknüpft wurde.[ 74 ]
Postmortem-Studien lieferten den ersten direkten Beweis für eine dopaminerge Dysfunktion im Gehirn und seiner anatomischen Lokalisation. Sie zeigten erhöhte Dopaminspiegel, dessen Metabolite und Rezeptoren im Striatum von Menschen mit Schizophrenie. [ 75 ], [ 76 ] An den Studien nahmen jedoch Patienten teil, die Antipsychotika erhielten. Daher war unklar, ob die Dysfunktion mit dem Beginn oder dem Endstadium der Erkrankung oder tatsächlich mit den Wirkungen der Antipsychotika zusammenhing.
 [ 77 ], [ 78 ], [ 79 ], [ 80 ], [ 81 ], [ 82 ], [ 83 ], [ 84 ], [ 85 ], [ 86 ]
[ 77 ], [ 78 ], [ 79 ], [ 80 ], [ 81 ], [ 82 ], [ 83 ], [ 84 ], [ 85 ], [ 86 ]
Dopamin und Dopamin
Es gibt also keinen Unterschied zwischen diesen Substanzen. Denn im Wesentlichen sind sie gleich. Diese Substanz wird im Körper produziert und fungiert als Neurotransmitter. Einfach ausgedrückt, hilft sie den Gehirnzellen, bestimmte Botschaften zu übermitteln. Im Volksmund wird diese Substanz als Glückshormon bezeichnet.
Die Dopaminproduktion führt zu einem Aktivitätsschub, guter Laune, hohem Energieniveau sowie verbessertem Gedächtnis und Aufmerksamkeit. Tatsächlich gibt es viele Vorteile. Es ist erwähnenswert, dass diese Substanz unter dem Einfluss von „Süßstoffen“ des Lebens produziert werden kann. Dies können sowohl Nahrung als auch körperliche Bewegung sein. Kurz gesagt: Was einen Menschen glücklich macht, stimuliert die Produktion dieses Hormons. Daher sollten Sie häufiger tun, was vollkommene Zufriedenheit bringt.
Dopamin und Dopamin sind dieselbe Substanz und erfüllen dieselbe Funktion. Es ist wichtig, den Spiegel des Glückshormons aufrechtzuerhalten, dann wird das Leben erfüllender.
Die Wirkung von Alkohol auf das Dopaminsystem
Dopaminerge Neuronen, die Informationen an die Hülle des Nucleus accumbens (NAc) weiterleiten, reagieren extrem empfindlich auf Alkohol. Studien an Ratten zeigten, dass beispielsweise Alkohol, der in Dosen von 2 bis 4 Milligramm pro Kilogramm Körpergewicht ins Blut gegeben wurde, die Dopaminausschüttung in der NAc-Hülle erhöhte und die chronische Selbstverabreichung von Alkohol unterstützte.[ 89 ] Bei Ratten stimulierte auch oraler Alkoholkonsum die Dopaminausschüttung im NAc.[ 90 ] Allerdings erfordert dieser Verabreichungsweg höhere Alkoholdosen, um den gleichen Effekt zu erzielen wie die direkte Injektion von Alkohol ins Blut.[ 91 ]
Die alkoholbedingte Stimulation der Dopaminfreisetzung in der NAc könnte die Aktivität einer anderen Kategorie von Neuromodulatoren erfordern: endogene Opioidpeptide. Diese Hypothese wird durch die Beobachtung gestützt, dass Chemikalien, die die Wirkung endogener Opioidpeptide hemmen (d. h. Opioidpeptidantagonisten), die Auswirkungen von Alkohol auf die Dopaminfreisetzung verhindern. Opioidpeptidantagonisten wirken primär auf die Hirnregion, in der dopaminerge Neuronen entstehen, die in die NAc projizieren. Diese Beobachtungen legen nahe, dass Alkohol die Aktivität endogener Opioidpeptide stimuliert und so indirekt zur Aktivierung dopaminerger Neuronen führt. Opioidpeptidantagonisten können diesen Prozess stören und dadurch die Dopaminfreisetzung reduzieren.
Die Wirkung von Alkohol als Verstärker: Die Rolle von Dopamin
Obwohl in zahlreichen Studien versucht wurde, die Rolle von Dopamin bei der Alkoholverstärkung durch Manipulation dopaminerger Signale aufzuklären, lassen diese Studien keine sicheren Schlussfolgerungen zu.[ 92 ] Ein Vergleich der Wirkungen von Alkohol mit den Wirkungen gängiger Verstärker wie Nahrungsmittel liefert jedoch einige Hinweise auf die Rolle von Dopamin bei der Vermittlung der Alkoholverstärkung.
Angenehme Nahrungsmittel aktivieren dopaminerge Signale in der NAc-Schale, indem sie beispielsweise bestimmte Sinnesreize (z. B. Geschmacks- oder Aromareize) liefern. Oral verabreichter Alkohol aktiviert auf ähnliche Weise Geschmacksrezeptoren und erhöht dadurch die Dopaminausschüttung in der NAc. Im Gegensatz zu Nahrungsmitteln kann Alkohol jedoch die Funktion dopaminerger Neuronen direkt verändern, sobald er das Gehirn erreicht. Dementsprechend beeinflusst oral eingenommener Alkohol die Dopaminausschüttung in der NAc sowohl durch seine geschmacklichen Eigenschaften (d. h. als herkömmlicher Verstärker) als auch durch seine direkten Auswirkungen auf das Gehirn (d. h. als Arzneimittelverstärker). In Übereinstimmung mit dieser Hypothese treten in der NAc zwei Spitzen der Dopaminausschüttung auf. Die erste Spitze resultiert aus den mit Alkohol verbundenen Geschmacksreizen, die zweite aus den Auswirkungen des Alkohols auf das Gehirn. Folglich kann die durch Alkohol induzierte direkte Aktivierung dopaminerger Signale die motivationalen Eigenschaften alkoholassoziierter Geschmacksreize verstärken. Durch diesen Mechanismus erhalten alkoholassoziierte Geschmacksreize starke Anreizeigenschaften (d. h. sie werden zu Motivationsreizen, die den Trinker zum Nachtrinken motivieren). Ebenso erhalten alkoholassoziierte Appetitreize (z. B. externe Reize wie das Erscheinen einer bestimmten Marke alkoholischer Getränke oder einer Bar) Anreizeigenschaften und fördern die Alkoholsuche und den Alkoholkonsum. Durch diese komplexen Mechanismen aktiviert die alkoholbedingte Dopaminausschüttung einen sekundären Verstärkungskreislauf, der den Alkoholkonsum fördert.
Die Rolle von Dopamin bei der Entwicklung einer Alkoholsucht
Die Dopaminfreisetzung in der NAc-Schale kann zur Entwicklung einer Alkoholabhängigkeit beitragen. Eine psychische Abhängigkeit von Alkohol entsteht, weil alkoholbedingte Reize übermäßige Motivationseigenschaften entwickeln, die ein starkes Verlangen nach alkoholischen Getränken (Craving) auslösen. Infolge dieses starken Verlangens verlieren normale Verstärker (z. B. Essen, Sex, Familie, Arbeit oder Hobbys) ihre Bedeutung und beeinflussen das Verhalten des Trinkers nur noch geringfügig.
Ein Mechanismus, der für die abnorme Bedeutung alkoholbedingter Reize verantwortlich sein könnte, ist die maladaptive Natur der alkoholbedingten Hochregulierung dopaminerger Signale im NAc. Wie bereits erwähnt, führt die durch normale Verstärker (z. B. Nahrung) induzierte verstärkte Dopaminausschüttung in der NAc-Schale rasch zur Gewöhnung, und die wiederholte Präsentation assoziierter Reize löst keine Dopaminausschüttung mehr aus. Im Gegensatz dazu tritt nach wiederholtem Alkoholkonsum keine Gewöhnung ein. Durch die anhaltende Dopaminausschüttung in der NAc-Schale als Reaktion auf Alkohol erhalten alkoholbedingte Reize eine abnorme emotionale und motivationale Bedeutung, was zu einer übermäßigen Kontrolle des Verhaltens des Trinkers führt. Diese übermäßige Kontrolle ist der Kern der Sucht.
 [ 93 ], [ 94 ], [ 95 ], [ 96 ], [ 97 ]
[ 93 ], [ 94 ], [ 95 ], [ 96 ], [ 97 ]
Rauchen und Dopamin
Tabakkonsumstörungen werden durch eine Vielzahl von Umwelt- und genetischen Faktoren beeinflusst. Umweltfaktoren decken ein breites Spektrum kultureller, sozialer und wirtschaftlicher Aspekte ab. Genetische Faktoren lassen sich in zwei Hauptgruppen unterteilen: Gene, die mit Stoffwechselwegen im Zusammenhang mit dem Nikotinstoffwechsel in Zusammenhang stehen und angeben, wie schnell jemand Nikotin zu Cotinin verstoffwechselt, und Gene, die mit der Belohnungskaskadentheorie in Zusammenhang stehen, also dem Ausmaß des Genusses beim Rauchen. Die wichtigsten Gene, die den Nikotinstoffwechsel beeinflussen, sind Cytochrom P450 CYP2A6 und CYP2B6. Zu den Genen, die die Belohnungskaskadentheorie beeinflussen, gehört ein komplexes Netzwerk aus Serotonin, Opioiden, Gamma-Aminobuttersäure (GABA) und Dopamin.[ 98 ]
Lesen Sie in diesem Artikel über Studien zu Dopamin-Kandidatengenen und Rauchen.
Wie kann man Dopamin erhöhen?
Tatsächlich ist dieser Prozess nicht kompliziert. Sie müssen versuchen, in Ihren Tagesplan die Aktivitäten aufzunehmen, die Freude bereiten können.
Aber das ist noch nicht alles. Es wird daher empfohlen, täglich Bananen zu essen. Sie enthalten eine Substanz, die Dopamin ähnelt. Kleine braune Flecken auf der Frucht enthalten eine größere Menge dieser nützlichen Substanz. Die Ernährung sollte mit Produkten angereichert sein, die Antioxidantien enthalten. Sie gehören zu den freien Radikalen, die den Dopaminspiegel erhöhen. Zu diesen Produkten gehören rote Bohnen, Preiselbeeren, Artischocken, Erdbeeren, Pflaumen und Blaubeeren.
Es ist sinnvoll, auf entkoffeinierten Kaffee zu verzichten, weniger Zucker zu konsumieren und den Konsum alkoholischer Getränke zu reduzieren. Es wird empfohlen, täglich eine Handvoll Mandeln zu essen. Sonnenblumenkerne sind ebenfalls geeignet. Es ist auch ratsam, Sesam zu essen. Er passt hervorragend zu jedem Salat und Sandwich mit frischem Gemüse.
Dopamin in Lebensmitteln
Dopamin spielt im menschlichen Körper eine wichtige Rolle bei der Koordination von Körperbewegungen, Motivation und Belohnung. Informationen über den Gehalt an Dopaminprodukten sind sehr begrenzt, möglicherweise aufgrund des mangelnden klinischen Interesses. Früchte der Gattung Musa, wie Bananen und Platanen, und die Art M. Persea americana (d. h. Avocado) enthalten hohe Dopaminspiegel. [ 102 ] Insbesondere wurden Dopaminspiegel in Bananenschalen (700 μg/g), Bananenmark (8 μg/g) und Avocados (4–5 μg/g) nachgewiesen. In Pflanzen spielt Dopamin eine schützende Rolle und ist an der reproduktiven Organogenese, Ionendurchlässigkeit, antioxidativen Aktivität [ 103 ] und der Bildung von Alkaloiden beteiligt. [ 104 ] Interessanterweise wurde gezeigt, dass die Blätter von Mucuna pruriens L. (d. h. Juckbohne) Dopamin enthalten, [ 105 ] und sind daher möglicherweise an der bekannten antiparkinsonischen Wirkung von aus den Samen gewonnenen Produkten beteiligt. [ 106 ] Geringe Konzentrationen wurden in Citrus sinensis L. (d. h. Orange), Malus sylvestris L. (d. h. Holzapfel), Tomaten, Auberginen, Spinat, Erbsen und Bohnen gemessen. Von episodischen Bewegungsstörungen (d. h. seitliches Kopfschütteln) wurde nach dem Genuss von Magermilch berichtet. Dieselben Autoren führten diese Wirkungen auf den hohen L-Tyrosin-Gehalt von Milchprodukten zurück. [ 107 ] Eine mögliche Wechselwirkung mit Dopamin kann jedoch nicht ausgeschlossen werden, die Daten aus der Literatur sind jedoch unzureichend.
Beachtung!
Um die Wahrnehmung von Informationen zu vereinfachen, wird diese Gebrauchsanweisung der Droge "Dopamin" übersetzt und in einer speziellen Form auf der Grundlage der offiziellen Anweisungen für die medizinische Verwendung des Medikaments präsentiert . Vor der Verwendung lesen Sie die Anmerkung, die direkt zu dem Medikament kam.
Beschreibung zu Informationszwecken zur Verfügung gestellt und ist kein Leitfaden zur Selbstheilung. Die Notwendigkeit für dieses Medikament, der Zweck des Behandlungsregimes, Methoden und Dosis des Medikaments wird ausschließlich durch den behandelnden Arzt bestimmt. Selbstmedikation ist gefährlich für Ihre Gesundheit.

