Facharzt des Artikels
Neue Veröffentlichungen
Kryptokokkenmeningitis
Zuletzt überprüft: 23.11.2021

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
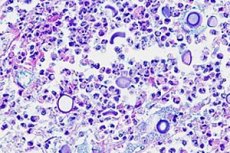
Eine Entzündung der weichen Membranen des Gehirns kann nicht nur durch Bakterien, Viren und Protisten, sondern auch durch eine Pilzinfektion verursacht werden. Eine Kryptokokken-Meningitis entwickelt sich, wenn die verkapselte Hefe Cryptococcus neoformans, die zu den humanen opportunistischen Krankheitserregern gehört, betroffen ist. [1] Sie wurde aufgrund ihrer Erstbeschreibung durch Otto Busse und Abraham Buschke im Jahr 1894 als Morbus Busse-Buschke bezeichnet. [2]
Nach ICD-10 lautet der Krankheitscode G02.1 (im Abschnitt über entzündliche Erkrankungen des Zentralnervensystems) sowie B45.1 im Abschnitt über Mykosen (also Pilzerkrankungen).
Epidemiologie
Acht von zehn Fällen von Kryptokokken-Meningitis betreffen Menschen mit HIV/AIDS.
Laut Daten, die von The Lancet Infectious Diseases im Frühjahr 2017 veröffentlicht wurden, verursacht dieser Pilz bei Menschen mit HIV oder AIDS jährlich etwa 220.000 Fälle von Kryptokokken-Meningitis, und mehr als 180.000 Menschen sterben. Die meisten Fälle von Kryptokokken-Meningitis treten in Afrika südlich der Sahara auf.
Laut WHO-Statistiken wurden im Jahr 2017 165,8 Tausend Fälle von Kryptokokken-Meningitis in Afrika, 43,2 Tausend in Asien, 9,7 Tausend in Amerika und 4,4 in europäischen Ländern registriert. Tausend Fälle der Krankheit.
Ursachen kryptokokkenmeningitis
Die Ursachen für diese Art von Meningitis sind Infektionen mit dem Pilz Cryptococcus neoformans (Klasse Tremellomycetes, Gattung Filobasidiella), der in der Umwelt lebt: im Boden (einschließlich Staub), auf verrottendem Holz, im Kot von Vögeln (Tauben) und Fledermäusen, usw.... Die Infektion erfolgt durch aerogene Mittel - durch Inhalation von Aerosol-Basidiosporen des Pilzes, obwohl C. Neoformans bei den meisten Menschen mit ausreichender Immunität nicht zur Entwicklung von Krankheiten führt und ein optionaler intrazellulärer opportunistischer Mikroorganismus bleibt (der andere Menschen nicht infizieren kann) ). Lesen Sie auch - Kryptokokken - die Erreger der Kryptokokkose [3]
In der Regel entwickelt sich eine Kryptokokkenmeningitis bei HIV-Infizierten (Stadium IVB) - als Sekundärinfektion sowie bei Menschen mit einem schlecht funktionierenden Immunsystem bei anderen Erkrankungen mit längerer Immunsuppression. [4]
Die Entzündung der Hirnhäute aufgrund von Kryptokokken wird als zerebrale oder extrapulmonale Form der Kryptokokkose angesehen , die nach hämatogener Verbreitung von C. Neoformans aus den Atemwegen und der Lunge in das Gehirn und das Rückenmark auftritt. [5]
Risikofaktoren
Die Faktoren mit dem größten Risiko für die Entwicklung einer Kryptokokken-Meningitis sind:
- Neugeborenenperiode (Neugeborenenperiode) und Frühgeburt von Säuglingen;
- Schwächung des Immunsystems bei Krebs (einschließlich Leukämie, multiplem Melanom, Lymphosarkom), bei Patienten mit HIV-Infektion und AIDS ;
- Diabetes;
- virale Hepatitis und andere Immunkomplex-Erkrankungen;
- Sichelzellenanämie;
- Chemotherapie bei Vorliegen einer onkologischen Diagnose;
- Überschreitung der zulässigen ionisierenden Strahlungsrate;
- lange Behandlungszyklen mit Antibiotika oder Steroiden;
- Installation von intravaskulären Kathetern und Shunts;
- Knochenmark oder Transplantation innerer Organe.
Pathogenese
Kryptokokken, die durch eine Polysaccharidkapsel vor menschlichen Immunzellen geschützt sind (unterdrückende Phagozytose), sezernieren Proteasen, Urease, Phospholipase und Nuklease, Enzyme, die Wirtszellen zerstören können. [6]
Und die Pathogenese der Kryptokokkose liegt darin, dass diese Enzyme Zellen durch Lyse von Membranen, Modifikation von Molekülen, Dysfunktion von Zellorganellen und Veränderungen des Zytoskeletts schädigen. [7]
Pilz-Serinproteasen zerstören Peptidbindungen von zellulären Proteinen, bauen Immunglobuline und Proteine von Immuneffektorzellen ab und C. Neoformans repliziert in mononukleären Phagozyten (Makrophagen), was deren Proliferation erleichtert. [8]
Darüber hinaus unterbrechen Kryptokokken die Integrität der Blut-Hirn-Schranke, indem sie Endothelzellen passieren und in infizierte Makrophagen übertragen werden. Der Pilz breitet sich über die Blutbahn in die Liquor cerebrospinalis und dann in die weichen Membranen des Gehirns aus, wobei sich im Hirngewebe "Kolonien" von Pilzzellen in Form von gelatinösen Pseudozysten bilden. [9]
Symptome kryptokokkenmeningitis
Die ersten Anzeichen einer Kryptokokkenmeningitis sind Fieber (Temperaturanstieg auf + 38,5-39 ° C) und starke Kopfschmerzen.
Klinische Symptome äußern sich auch in Übelkeit und Erbrechen, Krampfanfällen, Steifheit (Steifigkeit) des Nackens, erhöhter Lichtempfindlichkeit der Augen, Bewusstseins- und Verhaltensstörungen. [10]
Laut Experten entwickelt sich das meningeale Syndrom langsamer als bei einer bakteriellen Schädigung der Hirnhäute.
Komplikationen und Konsequenzen
Komplikationen und Folgen einer durch Cryptococcus verursachten Pilzmeningitis sind:
- signifikanter Anstieg des Hirndrucks;
- isolierte Schädigung der Hirnnerven mit Parese / Lähmung des Gesichts und atrophische Veränderungen des Sehnervs (die zu Augenproblemen führen);
- die Ausbreitung des Entzündungsprozesses auf das Gewebe des Subcortex und der Großhirnhemisphären - Kryptokokkenmeningoenzephalitis;
- Entwicklung eines Hirnabszesses (Kryptokokkoma);
- Erguss in den Subduralraum (unter der Dura mater);
- Rückenmarksverletzung;
- mentale Veränderungen und verminderte kognitive Funktionen.
Diagnose kryptokokkenmeningitis
Neben der Anamnese und ärztlichen Untersuchung umfasst die Diagnose einer C. Neoformans-Infektion bei Meningitis notwendigerweise Blutuntersuchungen: allgemeine klinische und biochemische, Blutserumanalyse auf Antikörper gegen C. Neoformans-Proteine, Blutkultur.
Es wird eine Lumbalpunktion durchgeführt und eine Analyse des Liquor cerebrospinalis auf Antigen und eine bakterioskopische Analyse (Bakterienkultur) des Liquor durchgeführt. [11]
Die instrumentelle Diagnostik erfolgt mittels Röntgen-Thorax und Magnetresonanztomographie des Gehirns.
Differenzialdiagnose
Differentialdiagnosen sind Meningitis und Meningoenzephalitis bakterieller und viraler Ätiologie, Hirnschädigung durch Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis oder Amöben (einschließlich Naegleria fowleri).
Behandlung kryptokokkenmeningitis
Die ätiologische Behandlung zielt auf die Ausrottung von Kryptokokken ab, für die Antimykotika verwendet werden.
Das Behandlungsschema umfasst die intravenöse Verabreichung (Tropfinfusion, über einen zentralen Venenkatheter oder peritoneale Infusion) eines antimykotischen Polyen-Antibiotikums Amphotericin B (Amphocyl) in Kombination mit dem Antimykotikum Flucytosin (5-Fluorocytosin) oder Fluconon, das eine fungizide und fungistatische Wirkung hat. Die Dosierung dieser Medikamente wird in Abhängigkeit vom Körpergewicht des Patienten berechnet.
Eine ständige Überwachung des Zustands des Patienten ist erforderlich, da Amphotericin B eine toxische Wirkung auf die Nieren hat und Nebenwirkungen von Flucytosin eine Hemmung der hämatopoetischen Funktion des Knochenmarks, Atem- oder Herzstillstand, die Entwicklung von Hautläsionen in der Form sein können der epidermalen Nekrolyse usw.
Nach den Empfehlungen der IDSA (Infectious Diseases Society of America) von 2010 hat sich die Behandlung seit zehn Jahren nicht geändert. Die antimykotische Erstlinienbehandlung basiert auf der Einleitung, Konsolidierung und Erhaltung der folgenden drei Patiententypen: [12]
Krankheiten im Zusammenhang mit HIV
- Induktionstherapie
- Amphotericin B-Desoxycholat (0,7-1,0 mg/kg/Tag) + Flucytosin (100 mg/kg/Tag oral) für 2 Wochen (A1-Nachweis)
- Liposomales Amphotericin B (3-4 mg / kg / Tag) oder Amphotericin B Lipidkomplex (5 mg / kg / Tag; Überwachung der Nierenfunktion) + Flucytosin (100 mg / kg / Tag) für 2 Wochen (Beweis B2)
- Amphotericin B-Desoxycholat (0,7 bis 1,0 mg / kg / Tag) oder liposomales Amphotericin B (3 bis 4 mg / kg / Tag) oder Amphotericin B-Lipidkomplex (5 mg / kg / Tag, für Patienten mit Flucytosin-Unverträglichkeit) für 4 bis 6 Wochen (Nachweis B2)
- Alternativen zur Induktionstherapie
- Amphotericin B-Desoxycholat + Fluconazol (B1-Nachweis)
- Fluconazol + Flucytosin (Beweis B2)
- Fluconazol (B2-Nachweis)
- Itraconazol (C2-Nachweis)
- Fluconazol (400 mg / Tag) für 8 Wochen (Daten A1)
- Fluconazol (200 mg / Tag) für 1 oder mehr Jahre (A1-Nachweis)
- Itraconazol (400 mg / Tag) für 1 oder mehr Jahre (Beweis C1)
- Amphotericin B-Desoxycholat (1 mg / kg / Woche) für 1 oder mehr Jahre (Evidenz C1)
- Konsolidierungstherapie
- Unterstützende Therapie
- Unterstützende Pflegealternativen
Transplantationsbedingte Krankheiten
- Induktionstherapie
- Liposomales Amphotericin B (3-4 mg/kg/Tag) oder Amphotericin B Lipidkomplex (5 mg/kg/Tag) + Flucytosin (100 mg/kg/Tag) für 2 Wochen (Beweis B3)
- Alternativen zur Induktionstherapie
- Liposomales Amphotericin B (6 mg / kg / Tag) oder Amphotericin B-Lipidkomplex (5 mg / kg / Tag) für 4-6 Wochen (Beweis B3)
- Amphotericin B-Desoxycholat (0,7 mg / kg / Tag) für 4-6 Wochen (Beweis B3)
- Fluconazol (400 bis 800 mg / Tag) für 8 Wochen (Beweis B3)
- Fluconazol (200 bis 400 mg / Tag) 6 Monate bis 1 Jahr (Beweis B3)
- Konsolidierungstherapie
- Unterstützende Therapie
Nicht-HIV-/Transplantations-bedingte Krankheit
- Induktionstherapie
- Amphotericin B-Desoxycholat (0,7 bis 1,0 mg/kg/Tag) + Flucytosin (100 mg/kg/Tag) für 4 Wochen oder länger (Beweis B2)
- Amphotericin B-Desoxycholat (0,7-1,0 mg / kg / Tag) für 6 Wochen (Beweis B2)
- Liposomales Amphotericin B (3-4 mg/kg/Tag) oder Amphotericin B Lipidkomplex (5 mg/kg/Tag) plus Flucytosin, 4 Wochen (Beweis B3)
- Amphotericin B-Desoxycholat (0,7 mg / kg / Tag) + Flucytosin (100 mg / kg / Tag) für 2 Wochen (Beweis B2)
- Konsolidierungstherapie
- Fluconazol (400 bis 800 mg / Tag) für 8 Wochen (Beweis B3)
- Fluconazol (200 mg / Tag) für 6-12 Monate (Beweis B3)
- Unterstützende Therapie
Die Kombination von Amphotericin B und Flucytosin erwies sich als die wirksamste Maßnahme zur Eliminierung von Infektionen und zeigte einen größeren Überlebensvorteil im Vergleich zu Amphotericin allein. Aufgrund seiner Kosten ist Flucytosin jedoch häufig nicht in Umgebungen mit begrenzten Ressourcen verfügbar, in denen die Krankheitslast erheblich ist. Die Kombination von Amphotericin B und Fluconazol wurde untersucht und erzielte die besten Ergebnisse im Vergleich zu einer mit Amphotericin B. [13], [14], [15]
Ohne Behandlung schreitet der klinische Verlauf zu Verwirrung, Krampfanfällen, Bewusstseinsstörungen und Koma fort.
Schmerzresistente Kopfschmerzen können nach adäquater bildgebender Untersuchung mit Computertomographie oder MRT mit spinaler Dekompression behandelt werden. Das sichere maximale Volumen an Liquor, das mit einer einzigen Lumbalpunktion abgelassen werden kann, ist unklar, aber bis zu 30 ml werden oft mit einer Druckkontrolle nach jeder 10 ml-Entnahme entfernt. [16]
Verhütung
Die Vorbeugung einer Infektion durch den Pilz Cryptococcus neoformans ist vor allem bei einem schwachen Immunsystem notwendig. [17]Es wird empfohlen, staubige Gebiete zu meiden und mit Land zu arbeiten, und HIV-positive Menschen sollten eine fortlaufende antiretrovirale Therapie erhalten.
Prognose
Ohne Behandlung ist die Prognose einer Pilzmeningitis schlecht.
Die anfängliche Prognose ist abhängig von den Prädiktoren der Mortalität, wie die folgenden [18], [19]:
- Der Öffnungsdruck des Liquor cerebrospinalis beträgt mehr als 25 cm Wasser. Kunst.
- Niedrige Anzahl weißer Blutkörperchen in der Liquor cerebrospinalis
- Sensorische Beeinträchtigungen
- Späte Diagnose
- Erhöhte Titer von Liquor-Antigenen
- Infektions-Clearance-Rate
- Die Hefemenge im Liquor überschreitet 10 mm 3 (übliche Praxis in Brasilien) [20]
- Nicht-HIV-Patienten und prognostische Faktoren bei diesen Patienten, zusätzlich zu den bereits erwähnten:
- Marker für eine schwache Entzündungsreaktion
- Keine Kopfschmerzen
- Schwere hämatologische bösartige Neubildung
- Chronische Nieren- oder Lebererkrankung
Die Sterblichkeit variiert von Land zu Land, abhängig von den Ressourceneinstellungen. In den Vereinigten Staaten und Frankreich bleibt sie hoch, mit 10-Wochen-Sterblichkeitsraten zwischen 15 und 26 % und bei HIV-freien Patienten aufgrund der späten Diagnose und dysfunktionalen Immunreaktionen sogar noch höher. Auf der anderen Seite steigt die Sterblichkeit in einer Umgebung mit begrenzten Ressourcen von 30 % auf 70 % in 10 Wochen aufgrund des verspäteten Zugangs zu medizinischer Versorgung und des fehlenden Zugangs zu Medikamenten, Manometern und optimaler Überwachung.

