Facharzt des Artikels
Neue Veröffentlichungen
Mukopolysaccharidose Typ 3
Zuletzt überprüft: 04.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
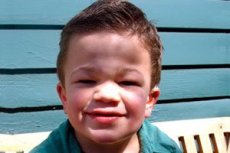
Mukopolysaccharidose, Typ III (Synonyme: Sanfilippo-Syndrom, lysosomaler aN-Acetylglucosaminidase-Mangel – Mukopolysaccharidose III A, Acetyl-CoA-a-Glucosaminid-N-Acetyltransferase-Mangel – Mukopolysaccharidose III B, N-Acetylglucosamin-6-sulfatase – Mukopolysaccharidose III C, Sulfamidase-Mangel – Mukopolysaccharidose III D).
Pathogenese
Die Krankheit wird durch Mutationen in vier verschiedenen Genen verursacht: lysosomale aN-Acetylglucosaminidase (Mukopolysaccharidose III A), Acetyl-CoA-a-Glucosaminid-N-Acetyltransferase (Mukopolysaccharidose III B), lysosomale N-Acetylglucosamin-6-sulfatase (Mukopolysaccharidose III C) und Sulfamidase (Mukopolysaccharidose III D). Alle Enzyme sind am Heparansulfat-Stoffwechsel beteiligt.
Das Heparan-N-Sulfatase-Gen (SGSH) befindet sich auf dem langen Arm des Chromosoms 17 – 17q25.3. 75,3 % der derzeit bekannten Mutationen im SGSH-Gen sind Punktmutationen. Es wurden häufige, für europäische Populationen charakteristische Mutationen beschrieben – R74C (56 % in Polen und 21 % in Deutschland) und R245H (56 % in den Niederlanden).
Die Häufigkeit der Mutation R74C beträgt 47,5 %, die der Mutation R245H 7,5 %. Die beiden anderen beschriebenen Mutationen, delll35G und N389S, machen zusammen 21,7 % der mutierten Allele aus.
Das Gen für aN-Acetyl-Glucosaminidase (NAGLU) befindet sich auf dem langen Arm von Chromosom 17 – 17q21. 69 % der im NAGLU-Gen gefundenen Mutationen sind Missense- und Nonsense-Mutationen, 26,3 % sind kleine Deletionen und Insertionen. Das Gen für Acetyl-CoA-cc-Glucosaminid-N-Acetyltransferase (HGSNAT) befindet sich auf dem kurzen Arm von Chromosom 8 – 8p11.1. Das Gen wurde erst 2006 charakterisiert, und bisher wurden nur wenige Mutationen darin gefunden.
Das Gen für die N-Acetyl-Glucosamin-6-Sulfatase (GNS) befindet sich auf dem langen Arm des Chromosoms 12 – 12ql4. Weltweit sind 12 Patienten mit Mukopolysaccharidose IIID registriert. Vier Mutationen im GNS-Gen wurden beschrieben.
Bei allen Subtypen der Mukopolysaccharidose III liegt eine Störung des Abbaus von Heparansulfat vor, das Teil der Struktur von Zellmembranen, einschließlich neuronaler Membranen, ist, was mit einem schweren neurodegenerativen Prozess korreliert, der durch kortikale Atrophie verursacht wird. Chronischer Durchfall wird durch die Beteiligung des autonomen Nervensystems am pathologischen Prozess zusammen mit einer Funktionsstörung der Darmschleimhaut erklärt. Sensorineuraler Hörverlust hat wahrscheinlich drei Ursachen: häufige Mittelohrentzündung, Deformation der Gehörknöchelchen und Anomalien des Innenohrs. Gelenksteifheit ist das Ergebnis einer Deformation der Metaphysen, die Verdickung der Gelenkkapsel ist sekundär zur Ablagerung von Glykosaminoglykanen und Fibrose. Intra-syndromale Unterschiede im Schweregrad der Erkrankung sind ausschließlich auf die verbleibende funktionelle Aktivität des mutierten Enzyms zurückzuführen: Je höher sie ist, desto milder ist die Erkrankung.
Symptome Mukopolysaccharidose Typ 3
Der klinische Polymorphismus beim Sanfilippo-Syndrom ist weniger ausgeprägt als bei anderen Formen der Mukopolysaccharidose. Charakteristisch sind ein langsamer Krankheitsverlauf, schwere neurologische Störungen mit leichten Symptomen der inneren Organe und anderer Systeme.
Die ersten Symptome der Krankheit treten meist im Alter zwischen 2 und 6 Jahren bei Kindern mit zuvor normaler Entwicklung auf. Zu den offensichtlichen Symptomen zählen eine Regression der psychomotorischen und sprachlichen Entwicklung, psychiatrische Störungen in Form eines Hyperaktivitätssyndroms, autistisches oder aggressives Verhalten, Schlafstörungen; Kinder werden nachlässig und unaufmerksam.
Weitere häufige Symptome sind Hirsutismus, grobes Haar, mäßige Hepatosplenomegalie, Valgusdeformität der Gliedmaßen und ein kurzer Hals. Die Entwicklung von groben Gesichtszügen wie Gargoylismus und Skelettdeformitäten wie multiple Dysostose ist bei Mukopolysaccharidose III im Vergleich zu anderen Arten von Mukopolysaccharidose, die durch den Hurler-Phänotyp gekennzeichnet sind, schwach ausgeprägt. Die Körpergröße entspricht in der Regel dem Alter, und Gelenksteifheit verursacht selten Funktionsstörungen. Die meisten Patienten entwickeln häufig Osteoporose und Osteomalazie. Sekundäre Skeletterkrankungen - ein hohes Risiko für pathologische Frakturen. Schwere psychoneurologische Störungen werden am häufigsten im 6.-10. Lebensjahr beobachtet, sie führen zu ausgeprägter sozialer Fehlanpassung. Progressiver sensorineuraler Hörverlust ist allen Patienten mit schweren und mittelschweren Formen der Erkrankung inhärent. Im Verlauf der Erkrankung werden bei fast allen Patienten Krämpfe beobachtet.
Die Krankheit schreitet rasch voran und die meisten Patienten erreichen nicht das 20. Lebensjahr. Mukopolysaccharidose IIIA gilt als die häufigste und schwerwiegendste Form dieses Syndroms.
Diagnose Mukopolysaccharidose Typ 3
Die Diagnose einer Mukopolysaccharidose III wird durch die Bestimmung der Glykosaminoglykanausscheidung im Urin und die Messung der Enzymaktivität bestätigt. Bei Mukopolysaccharidose III ist die Gesamtausscheidung von Glykosaminoglykanen im Urin erhöht und es kommt zu einer Hyperausscheidung von Heparansulfat. Die Aktivität lysosomaler Enzyme, die einem bestimmten Subtyp der Mukopolysaccharidose III entsprechen, wird in Leukozyten- oder Hautfibroblastenkulturen mithilfe eines künstlichen fluoreszierenden Substrats gemessen.
Pränatale Diagnostik ist durch Messung der Enzymaktivität in der Chorionzottenbiopsie in der 9.–11. Schwangerschaftswoche und/oder durch Bestimmung des Glykosaminoglykanspektrums im Fruchtwasser in der 20.–22. Schwangerschaftswoche möglich. Bei Familien mit bekanntem Genotyp kann eine DNA-Diagnostik in der Frühschwangerschaft durchgeführt werden.
Welche Tests werden benötigt?
Differenzialdiagnose
Die Differentialdiagnostik erfolgt sowohl innerhalb der Gruppe der Mukopolysaccharidosen als auch bei anderen lysosomalen Speicherkrankheiten: Mukolipidosen, Galaktosialidose, Sialidose, Mannosidose, Fucosidose, GM1-Gangliosidose.
Wen kann ich kontaktieren?
Behandlung Mukopolysaccharidose Typ 3
Bislang wurden keine wirksamen Therapiemethoden für Mukopolysaccharidose III entwickelt. Eine symptomatische Therapie ist angezeigt.
Использованная литература


 [
[