Neue Veröffentlichungen
Neues Gerät verbessert die Erzeugung von Stammzellen für die Alzheimer-Therapie
Zuletzt überprüft: 02.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.

Forscher in Schweden geben an, eine Technik zur Umwandlung gewöhnlicher Hautzellen in neurale Stammzellen perfektioniert zu haben. Dies bringe sie ihrer Aussage nach einer Entwicklung kostengünstiger personalisierter Zelltherapien für die Alzheimer- und Parkinson-Krankheit näher.
Mithilfe eines speziell entwickelten Mikrofluidikgeräts hat das Forschungsteam einen beispiellosen und beschleunigten Ansatz entwickelt, um menschliche Hautzellen in induzierte pluripotente Stammzellen (iPSCs) umzuprogrammieren und diese dann in neurale Stammzellen umzuwandeln.
Der Erstautor der Studie, Saumya Jain, sagt, die Plattform könne die Zelltherapie verbessern und ihre Kosten senken, indem sie die Verträglichkeit und Akzeptanz der Zellen im Körper des Patienten verbessere. Die Studie wurde von Wissenschaftlern des KTH Royal Institute of Technology in der Fachzeitschrift Advanced Science veröffentlicht.
Anna Herland, leitende Autorin der Studie, sagte, die Studie habe den ersten Einsatz von Mikrofluidik demonstriert, um iPSCs in die Umwandlung neuronaler Stammzellen zu lenken.
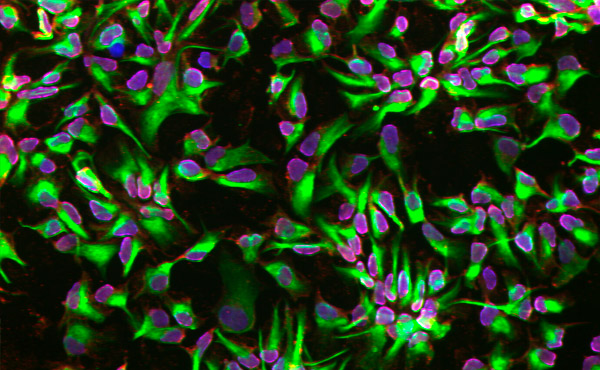
Differenzierte neuronale Stammzellen mithilfe einer mikrofluidischen Plattform. Foto: KTH Royal Institute of Technology
Die Umwandlung normaler Zellen in neurale Stammzellen erfolgt in zwei Schritten: Zunächst werden die Zellen biochemischen Signalen ausgesetzt, die sie dazu anregen, sich in pluripotente Stammzellen (iPSCs) zu verwandeln, die wiederum unterschiedliche Zelltypen hervorbringen können.
Anschließend werden sie in eine Kultur überführt, die die Signale und Entwicklungsprozesse des Nervensystems nachahmt. Dieser Schritt, die sogenannte neuronale Differenzierung, lenkt die Zellen in Richtung ihrer Entwicklung zu neuronalen Stammzellen.
Im letzten Jahrzehnt hat sich die Laborumgebung für diese Art von Arbeit schrittweise von herkömmlichen Tablets zu mikrofluidischen Geräten verlagert. Laut Herland stellt die neue Plattform eine Verbesserung der Mikrofluidik für beide Schritte dar: die iPSC-Generierung und die Differenzierung neuronaler Stammzellen.
Mithilfe von Zellen aus menschlichen Hautbiopsien stellten die Forscher fest, dass die Mikrofluidik-Plattform die Differenzierung der Zellen zu einem neuronalen Schicksal in einem früheren Stadium beschleunigte als dies bei Zellen der Fall war, die in herkömmlichen Platten differenziert wurden.
„Wir haben dokumentiert, dass die begrenzte Umgebung der Mikrofluidik-Plattform die Entwicklung neuronaler Stammzellen fördert“, sagt Herland.
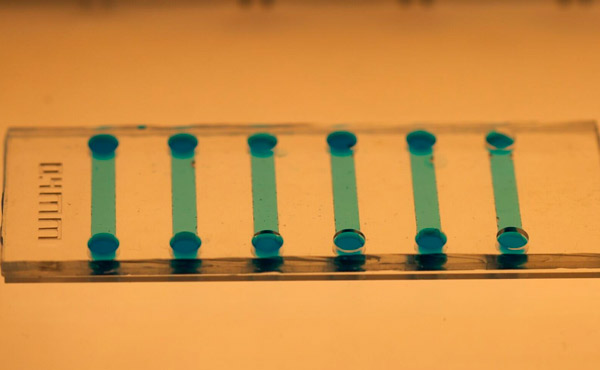
Nahaufnahme des Mikrofluidik-Chips zur Stammzellinduktion. Foto: KTH Royal Institute of Technology
Jain sagt, dass sich der Mikrofluidik-Chip mithilfe von Polydimethylsiloxan (PDMS) leicht herstellen lässt und dass seine mikroskopische Größe erhebliche Einsparungen bei Reagenzien und Zellmaterial ermöglicht.
Die Plattform lasse sich leicht modifizieren, um die Differenzierung in andere Zelltypen zu ermöglichen, fügt er hinzu. Sie sei automatisierbar und biete ein geschlossenes System, das Konsistenz und Zuverlässigkeit bei der Produktion hochhomogener Zellpopulationen gewährleiste.
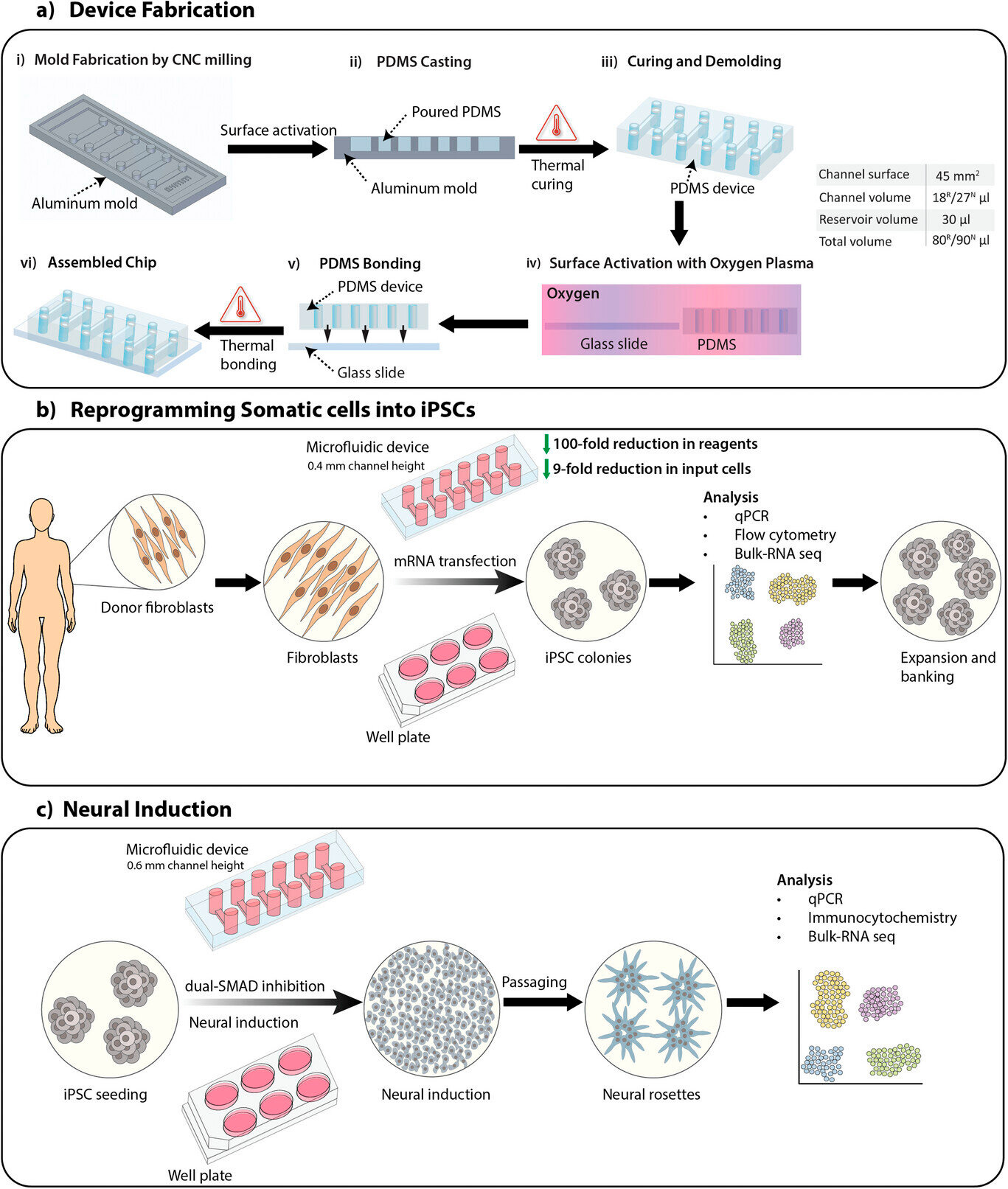
Überblick über die Studie, einschließlich Geräteherstellung, Reprogrammierung somatischer Zellen zu induzierten pluripotenten Stammzellen (iPSCs) und neuronaler Induktion von iPSCs mittels des SMAD-Protokolls zur Erzeugung neuronaler Stammzellen.
A) Herstellungsprozess eines mikrofluidischen Geräts mit 0,4 mm und 0,6 mm hohen Kanälen für die Reprogrammierung somatischer Zellen (R) bzw. neuronale Induktion (N). Kanalvolumina und Gesamtvolumen sind in der Tabelle aufgeführt.
B) Überblick über den Reprogrammierungsprozess somatischer Zellen zu iPSCs auf mikrofluidischen Geräten und Platten mittels mRNA-Transfektion.
C) Überblick über den neuronalen Induktionsprozess von iPSCs zu neuronalen Stammzellen auf mikrofluidischen Geräten und Platten mittels des SMAD-Protokolls.
Quelle: Advanced Science (2024). DOI: 10.1002/advs.202401859
„Dies ist ein Schritt in Richtung der Ermöglichung personalisierter Zelltherapien für Alzheimer und Parkinson“, fügt Jain hinzu.
An der Studie waren auch Wissenschaftler des Karolinska Institutet und der Universität Lund beteiligt, die im IndiCell-Konsortium zusammenarbeiteten.
