Neue Veröffentlichungen
„Sauerstoff für die Zellen“: Ein einfaches Implantat half, den Zuckerspiegel ohne starke Medikamente zu senken
Zuletzt überprüft: 18.08.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Ein neues „Sauerstoffimplantat“ zur Behandlung von Typ-1-Diabetes wurde in Nature Communications beschrieben: Ein kompakter elektrochemischer Sauerstoffgenerator (iEOG) versorgt eine Makrokapsel mit insulinproduzierenden Zellen kontinuierlich mit Sauerstoff. Dieses System ermöglicht eine dichte Packung isolierter Inselzellen (bis zu 60.000 IEQ/ml) und erhält deren Lebensfähigkeit und Sekretion auch bei niedrigem Sauerstoffgehalt. Bei diabetischen Ratten hielt das unter die Haut implantierte Gerät den Blutzuckerspiegel bis zu drei Monate lang normal – ohne Immunsuppression. Kontrollratten blieben ohne Sauerstoff hyperglykämisch.
Hintergrund
- Das größte technische Problem ist der Sauerstoff. Sobald wir die Zellen hinter der Membran „verstecken“ und das Gerät unter die Haut legen (was bequem und einfach zu entnehmen ist), fehlt ihnen Sauerstoff: Die Diffusion durch die Membran und die schlecht durchblutete Stelle entspricht nicht den Bedürfnissen der „gefräßigen“ Inseln. Daher der frühe Tod, die schwache Arbeit und die Notwendigkeit, die Aussaat stark auszudünnen - sonst wird die Kapsel riesig.
- Warum ist es physikalisch so schwierig? Sauerstoff durchdringt Gewebe nur über sehr kurze Distanzen, und eingekapselte Zellen haben keine eigenen Gefäße – in den ersten Monaten leben sie nur durch passive Diffusion. Jede Verdickung des Materials oder „Verdichtung“ der Zellen führt schnell zu Hypoxie im Zentrum der Kapsel.
- Was haben Sie vorher versucht?
- Sie stellten sauerstoffnachfüllbare Makrogeräte her (z. B. βAir): Im Inneren befindet sich ein Reservoir, das täglich mit Sauerstoff aufgefüllt wird; es gab präklinische und frühe klinische Studien. Es funktioniert, ist aber für den Patienten arbeitsintensiv.
- Es wurden chemische O₂-Donatoren und Trägermaterialien (Perfluorverbindungen) ausprobiert. Sie helfen zwar, haben aber nur eine kurze und schwer kontrollierbare Wirkung. Es wurden auch „Luft“-Rahmen entwickelt, um die O₂-Zufuhr in die Gelschicht zu beschleunigen.
- Die Kapseln selbst und die Implantationsstellen (dünne Membranen, Prävaskularisierung) wurden verbessert, stoßen aber ohne externe O₂-Quelle immer noch an die Grenzen der Zelldichte.
- Welche Lücke im Puzzle füllt die neue Arbeit? Die Autoren von Nature Communications zeigen eine kontinuierliche Sauerstoffversorgung durch einen Minigenerator direkt im Inneren des Makroverkapselungssystems: Das Gerät entzieht dem Gewebe Wasser und setzt elektrochemisch O₂ frei, das gleichmäßig durch die Zellkapsel „atmet“. Die Idee ist, der Kapsel einen „eigenen Aquariumkompressor“ zu geben, damit sie mehr Zellen verpacken und diese dennoch am Leben und funktionsfähig halten kann – selbst an einer subkutanen, nicht sehr „sauerstoffreichen“ Stelle.
Warum ist das überhaupt notwendig?
Die Inselzell- oder Betazelltransplantation ist einer der vielversprechendsten Wege zur „funktionellen Heilung“ von Typ-1-Diabetes. Es gibt jedoch zwei große Hindernisse:
- Immunität – erfordert normalerweise lebenslange Immunsuppressiva;
- Sauerstoffmangel – Kapseln, die das Immunsystem schützen, trennen gleichzeitig Zellen von den Gefäßen, und die nach Sauerstoff lechzenden Betazellen „ersticken“ schnell. Die neue Arbeit stößt an die zweite Hürde: Sie versorgt die Kapsel mit einer eigenen, kontrollierten Sauerstoffquelle.
So funktioniert das Implantat
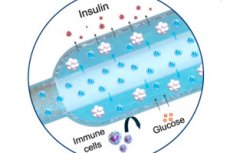
- Zwei Teile. In einem Titangehäuse befindet sich ein Mini-Sauerstoffgenerator (iEOG), der der interstitiellen Flüssigkeit Wasser entzieht und durch Elektrolyse O₂ freisetzt; daneben befindet sich eine dünne, lineare Kapsel mit Zellen (ähnlich einer langen „Wurst“), durch die ein gasdurchlässiger Schlauch verläuft: Sauerstoff wird gleichmäßig entlang der gesamten Kapsel absorbiert. Zwischen den Zellen und Geweben befindet sich eine semipermeable Membran (Elektrospin + Alginat): Glukose und Insulin passieren sie, Immunzellen nicht.
- Abmessungen: Die zweite Version des iEOG hat einen Durchmesser von 13 mm, eine Dicke von 3,1 mm und ein Gewicht von etwa 2 g. In Kombination mit einer Kapsel kann ein solches System durch einen kleinen Einschnitt eingeführt und entfernt werden, was für die Sicherheit wichtig ist.
- Produktivität. Der Generator erzeugt ca. 1,9–2,3 cm³ O₂/h und hält den angegebenen Durchfluss über Monate und sogar Jahre aufrecht (in Langzeittests in einer Kochsalzlösung – bis zu 2,5 Jahre). Nach der Implantation in Ratten blieb dieser Wert erhalten. Ein solcher Durchfluss deckt den Bedarf von Hunderttausenden von Inseläquivalenten – die Größenordnung, die ein Mensch benötigt.
Was die Experimente zeigten
- In vitro: Bei 1 % O₂ (schwere Hypoxie) blieb durch die Sauerstoffversorgung die Lebensfähigkeit und Sekretion in INS-1-Aggregaten und in menschlichen Inselzellen erhalten, die in einer sehr dichten Schicht (60.000 IEQ/ml) gepackt waren.
- In vivo (Ratten). Nach subkutaner Implantation in einem allogenen Diabetesmodell normalisierte das iEOG-System die Glykämie für bis zu drei Monate ohne Immunsuppression; Geräte ohne Sauerstoff zeigten keine Wirkung. Die Histologie um den Generator herum zeigte keine signifikanten Nebenwirkungen.
Warum ist das für die Klinik wichtig?
- Ein Schritt in Richtung „realistischer Dimensionen“. Um einem Erwachsenen eine Dosis von 300.000 bis 770.000 IEQ zu verabreichen, muss die Kapsel dicht gepackt sein – dies wurde bisher durch Sauerstoff begrenzt. Eine kontrollierte Sauerstoffzufuhr hebt die Dichtegrenze auf und ermöglicht es, das Gerät kompakt genug für eine echte Implantation zu gestalten.
- Plus Komfort. Zuvor haben wir chemische Sauerstoffspender (Peroxide) ausprobiert – sie wirken nicht lange und sind unkontrollierbar, sowie O₂-Reservoirs mit täglichem „Nachfüllen“ durch die Haut – umständlich und unbequem. Hier wird Sauerstoff ständig und in dosierten Dosen zugeführt, ohne Injektionen.
Technische Details, die überzeugen
- Die Wasserquelle ist das Gewebe. iEOG nimmt den Dampf der interstitiellen Flüssigkeit durch ein poröses „Fenster“ auf und trennt dann mithilfe einer klassischen Membran-Elektroden-Einheit (MEA) und einer Spannung von 1,4–1,8 V Wasser in H₂ und O₂; Gase werden über verschiedene Kanäle entfernt.
- Haltbarkeit. Drei Geräte in Kochsalzlösung funktionierten 11 Monate, 2 Jahre und 2,5 Jahre lang mit Gleichstrom, ohne dass es durch Sauerstoffzufuhr zu Leistungseinbußen kam. Nach der Implantation in immundefiziente und immunkompetente Ratten blieb die Leistung erhalten.
Einschränkungen und „Was kommt als Nächstes?“
Dies ist noch vorklinisch: Ratten, hohe Dichte in der Kapsel, Sauerstoffversorgung – alles ist großartig, aber wichtige Tests stehen noch bevor:
- Skalierung auf menschliche Dosen und Zeitrahmen;
- Zuverlässigkeit und Stromversorgung von Elektrochemikern im menschlichen Körper über Jahre hinweg (die Architektur der Stromversorgung wird im Artikel nicht detailliert beschrieben);
- Minimierung der Fibrose um die Kapseln und Diffusionsstabilität;
- Tests an Beta-Stammzellen und in menschenähnlicheren Modellen. Die Autoren vergleichen ihre Lösung offen mit früheren Ansätzen und positionieren sie als Plattform für klinisch übertragbare Kapseln.
Abschluss
Damit transplantierte Betazellen ohne Immunsuppressiva überleben und funktionieren können, müssen sie atmen. Das Team von Cornell und seinen Partnern zeigte, dass ein in eine lineare Kapsel eingebauter Mini-Sauerstoffgenerator die Zellen ausreichend lange und gleichmäßig mit Sauerstoff versorgen kann, um eine hohe Sauerstoffdichte zu überstehen und den Blutzuckerspiegel auch subkutan zu senken. Bis zur klinischen Anwendung ist es noch ein weiter Weg, aber die technische Logik ist einfach und überzeugend: Zellen dort Luft geben, wo sie fehlt.
