Neue Veröffentlichungen
Neuroprothese für den Magen-Darm-Trakt: Stellt die Peristaltik wieder her und aktiviert „Sättigungshormone“
Zuletzt überprüft: 18.08.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Gastrointestinale Motilitätsstörungen (Speiseröhre und Magen) – Achalasie, Gastroparese, Dysphagie usw. – betreffen mehr als 20 % der Bevölkerung und verursachen erhebliche Morbidität und Kosten. Standardansätze – Medikamente, Verhaltensinterventionen und Operationen – sind oft nur begrenzt wirksam und stellen die koordinierte Peristaltik nicht wieder her.
- Warum bestehende Geräte das Problem nicht lösen. Die elektrische Stimulation des Magen-Darm-Trakts wird seit den 1960er Jahren untersucht, doch klinisch zugelassene Implantate (z. B. Enterra bei Gastroparese, VBLOC-Vagusstimulatoren bei Adipositas, InterStim-Sakralstimulation bei Stuhlinkontinenz) arbeiten überwiegend im offenen Kreislauf und haben oft inkonsistente Auswirkungen auf die Magenentleerung. Der Grund dafür ist, dass eine oder mehrere Stromquellen mit konstanten Parametern die räumlich-zeitliche Komplexität der natürlichen Peristaltik nicht reproduzieren.
- Physiologie, die „imitiert“ werden muss. Die Peristaltik ist ein geschlossener Kreislauf: sensorische Signale (Dehnung, Temperatur, chemische Reize) → Reflexreaktionen im Plexus myentericus und der glatten Muskulatur. Neben dem Nahrungstransport beeinflusst die Motilität afferente Darm-Hirn-Signale und Sättigungshormone (GLP-1, Insulin, Ghrelin) und erzeugt so Appetit und Sättigungsgefühl. Bei Motilitätsstörungen sind diese Kreisläufe gestört.
- Technologische Lücke. Um die „richtigen“ Wellen zu reproduzieren, ist eine Mehrkanalstimulation direkt in der Nähe des Plexus myentericus und der Muskelschicht erforderlich. Der Zugang dorthin erfordert jedoch in der Regel einen invasiven Eingriff; fortgeschrittene endoskopische Techniken (z. B. NOTES) sind komplex und wenig verbreitet. Es werden minimalinvasive Instrumente benötigt, die eine präzise Platzierung der Elektroden in der Submukosa ermöglichen und in einem geschlossenen Kreislauf „Sensorik → Stimulation“ arbeiten.
- Was die neue Arbeit bietet. Die Autoren beschreiben eine endoskopisch installierte, mehrkanalige Neuroprothese mit elektrischer und chemischer Stimulation, die koordinierte peristaltische Wellen auslösen kann, sobald ein Signal über den Durchgang eines Bolus vorliegt. Dadurch wird nicht nur die Motilität wiederhergestellt, sondern auch die Stoffwechselreaktion moduliert (und nähert sich einem „gesättigten“ Zustand an). Dies schließt wichtige Lücken: Zugang zur gewünschten Schicht, räumlich-zeitliche Koordination und Arbeit in einem geschlossenen Kreislauf.
Kurz gesagt: Es gibt eine große klinische Nische – weit verbreitete, schlecht behandelte Desmotivationen. Bisherige „offene“ Stimulanzien ahmen die natürliche Physiologie nicht nach. Daher ist es logisch, dem Implantat beizubringen, „wie der Magen-Darm-Trakt zu denken“: den Bolus zu erfassen und die physiologische Peristaltik genau dort auszulösen, wo das natürliche Signal verläuft – am Plexus myentericus.
Ein Team des MIT, Harvard und Brigham entwickelte ein Miniatur-Speiseröhren-/Magenimplantat, das Nahrungsbolus in einem geschlossenen Kreislauf erkennt und koordinierte Peristaltikwellen auslöst. Bei Schweinen stellte das Gerät nicht nur die Speiseröhren- und Magenmotilität wieder her, sondern löste auch hormonelle Veränderungen ähnlich dem postprandialen Zustand (nach dem Essen) aus. Das Implantat wird endoskopisch eingesetzt, ohne Bauchoperation. Die Studie wurde in der Fachzeitschrift Nature veröffentlicht.
Was haben sie sich ausgedacht?
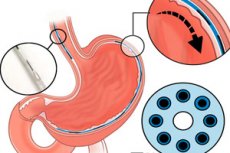
- Das Implantat selbst. Eine dünne „faserige“ Neuroprothese mit einem Durchmesser von ≈1,25 mm mit sieben Elektroden alle 1 cm und einem Mikrokanal zur lokalen Verabreichung von Substanzen (Elektro- und Chemostimulation). Seine Flexibilität und Abmessungen ermöglichen das Einführen durch einen Standard-Instrumentenkanal eines Endoskops (2,8–3,2 mm).
- Installation. Es wurde ein endoskopisches Instrument entwickelt: eine Nadel mit einem Rückwärtszug eines Nitinol-„Hakens“, Hydrodissektion und der entscheidende Trick – die Suche nach der Submukosa durch Gewebeimpedanz für eine präzise Platzierung direkt über der Muskelschicht, in der Nähe des Plexus myentericus.
- Geschlossener Kreislauf. Das System liest das Bolussignal (EMG/intraluminale Sensoren) und wählt ein Stimulationsmuster aus, um sequentielle Kontraktionen ähnlich der natürlichen Peristaltik auszulösen. Es ist möglich, „erregende“ und „hemmende“ Reize zu kombinieren sowie die Schließmuskeln durch Mikrodosen von Medikamenten lokal zu entspannen.
Was wurde an Tieren gezeigt
- Speiseröhre: Das Implantat erzeugte „Schluckwellen“, ohne dass tatsächlich geschluckt werden musste, einschließlich einer kontrollierten Entspannung des unteren Ösophagussphinkters (durch Mikroverabreichung von Glukagon) und programmierbarer Vorwärts-/Rückwärtswellen – im Wesentlichen ein peristaltischer „Joystick“.
- Magen. Nach 20 Minuten Stimulation erhöhte sich die Peristaltikfrequenz im Vergleich zur Kontrolle etwa um das Zweifache (n≈4, p<0,05).
- Metabolische „Sättigungsillusion“. Unter Fastenbedingungen führte eine 30-minütige Stimulation (Speiseröhre oder Magen) zu hormonellen Veränderungen: einem Anstieg von GLP-1 und Insulin, einem Abfall von Ghrelin (Appetithormon); bei Magenstimulation wurde auch ein Anstieg von Glucagon festgestellt. Das Profil ähnelte insgesamt dem postprandialen Zustand.
Sicherheits- und Konstruktionsdetails
Kurze In-vitro-Biokompatibilitätstests (Materialextrakte) zeigten keine Toxizität; in vivo 7 Tage nach der Implantation zeigte sich eine normale Wanddehnbarkeit und keine Gerätemigration/grobe Gewebeschädigung. (Die weitere Haltbarkeit und Zuverlässigkeit erfordern Langzeittests.)
Warum ist das notwendig?
- Motilitätsstörungen und refraktäre Zustände. Achalasie, Gastroparese, Dysphagie, postoperative Störungen – hier erzielen klassische Medikamente/Operationen oft nur eine unzureichende Wirkung. Die lokale Mehrkanalstimulation kommt der realen Physiologie näher als bestehende „Einkanal“-Implantate mit offenem Regelkreis.
- Stoffwechselstörungen. Durch die Kontrolle der afferenten Darm-Hirn-Bahnen könnte das Gerät möglicherweise Appetit und Stoffwechsel modulieren, was für Fettleibigkeit/Diabetes interessant ist (bisher Hypothese, keine Beweise beim Menschen).
Einschränkungen und was als nächstes kommt
Dies sind präklinische Arbeiten an Schweinen im akuten und subakuten Modus. Es folgen Langzeitstudien zu Kontaktstabilität, Energieversorgung, Fibroserisiko, präzisen Stimulationsprotokollen und anschließend erste klinische Studien an Patienten mit schweren Formen von Bewegungsstörungen. Es wurde jedoch bereits gezeigt, dass die Peristaltik auf Befehl „eingeschaltet“ und hormonelle Reaktionen in Richtung Sättigung verschoben werden können – und das alles durch endoskopischen Zugang.
