Neue Veröffentlichungen
Protein für genetische Entzündungskrankheit identifiziert
Zuletzt überprüft: 02.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Ein Forscherteam um Dr. Hirotsugu Oda vom Exzellenzcluster für Alternsforschung CECAD der Universität zu Köln hat die Rolle eines bestimmten Proteinkomplexes bei bestimmten Formen der Immundysregulation entdeckt. Dieses Ergebnis könnte zur Entwicklung neuer Therapieansätze führen, die darauf abzielen, die Autoinflation zu reduzieren und das Immunsystem von Patienten mit einer genetischen Fehlfunktion dieses Proteinkomplexes wiederherzustellen.
Der lineare Ubiquitin-Assemblierungskomplex (LUBAC), bestehend aus den Proteinen HOIP, HOIL-1 und SHARPIN, ist seit langem für seine entscheidende Rolle bei der Aufrechterhaltung der Immunhomöostase bekannt. Frühere Studien an Mäusen zeigten die schwerwiegenden Folgen des SHARPIN-Verlusts, der zu schwerer Dermatitis durch übermäßiges Absterben von Hautzellen führte. Die spezifischen gesundheitlichen Folgen eines SHARPIN-Mangels beim Menschen blieben jedoch unklar.
Das Forschungsteam berichtete erstmals über zwei Personen mit SHARPIN-Mangel, die Symptome von Autoinflation und Immunschwäche zeigten, aber unerwarteterweise keine dermatologischen Probleme zeigten, wie dies bei Mäusen der Fall war.
Bei weiteren Untersuchungen stellte sich heraus, dass diese Personen eine beeinträchtigte kanonische NF-κB-Reaktion, einen wichtigen Signalweg der Immunantwort, aufwiesen. Sie zeigten zudem eine erhöhte Anfälligkeit für Zelltod durch Mitglieder der Tumornekrosefaktor-Superfamilie (TNF). Die Behandlung eines SHARPIN-defizienten Patienten mit einer Anti-TNF-Therapie, die spezifisch den TNF-induzierten Zelltod hemmt, führte zu einer vollständigen Rückbildung der Autoinflation auf zellulärer Ebene und im klinischen Erscheinungsbild.
Die Studie zeigt, dass übermäßiger und unkontrollierter Zelltod eine entscheidende Rolle bei genetisch bedingten Entzündungskrankheiten des Menschen spielt. Odas Team hat den SHARPIN-Mangel als neues Mitglied einer Gruppe genetisch bedingter Entzündungskrankheiten des Menschen aufgenommen, die sie als „angeborene Zelltodfehler“ bezeichnen.
Schutz vor Immunschwäche Die Studie wurde im Labor von Dr. Dan Kastner an den National Institutes of Health (NIH) in den USA durchgeführt. Die Wissenschaftler dort hatten Gelegenheit, einen Patienten zu beobachten, der bereits im Kindesalter unter unerklärlichen Fieberschüben, Arthritis, Kolitis und Immunschwäche litt.
Nach Einholung der Einwilligungserklärung führten sie eine Exomsequenzierung des Patienten und seiner Angehörigen durch und stellten fest, dass der Patient eine verheerende genetische Variante im SHARPIN-Gen aufwies, die zu nicht nachweisbaren SHARPIN-Proteinwerten führte. Sie stellten außerdem fest, dass die Zellen des Patienten sowohl in Zellkulturen als auch in Biopsien eine erhöhte Absterbeneigung zeigten.
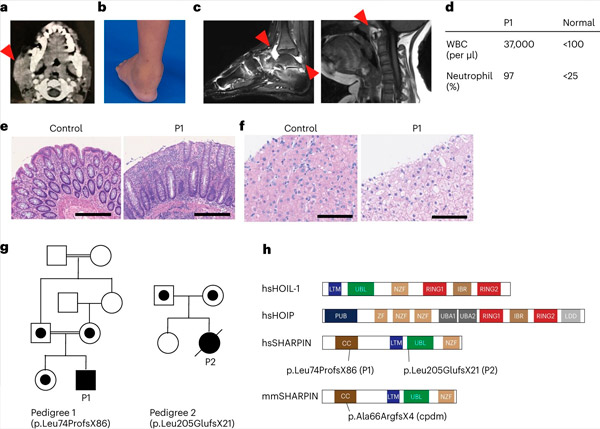
SHARPIN-Mangel verursacht beim Menschen Autoinflammation und Leberglykogenose. Quelle: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Das Team stellte außerdem fest, dass die Entwicklung lymphatischer Keimzentren – spezialisierte Mikrostrukturen in den Rachenmandeln, die für die Reifung der B-Zellen unseres Immunsystems und damit für die Antikörperproduktion entscheidend sind – aufgrund des erhöhten B-Zell-Todes deutlich reduziert war. Diese Ergebnisse erklären die Immunschwäche der Patienten und unterstreichen die wichtige Rolle von LUBAC bei der Aufrechterhaltung der Immunhomöostase beim Menschen.
„Unsere Studie unterstreicht die entscheidende Bedeutung von LUBAC für den Schutz vor Immundysregulation. Indem wir die molekularen Mechanismen aufklären, die dem LUBAC-Mangel zugrunde liegen, ebnen wir den Weg für neue therapeutische Strategien zur Wiederherstellung der Immunhomöostase“, sagte Oda, der Hauptautor der Studie.
Er fügte hinzu: „Einer der Patienten mit SHARPIN-Mangel war bereits jahrelang an den Rollstuhl gefesselt, bevor wir ihn zum ersten Mal sahen. Seine Knöchel waren entzündet, und das Gehen war zu schmerzhaft. Die genetische Diagnose ermöglichte es uns, den richtigen molekularen Signalweg zu finden, der seiner Erkrankung zugrunde liegt.“
Seit Beginn der Anti-TNF-Therapie ist der Patient seit fast sieben Jahren beschwerdefrei. „Als Kliniker und Wissenschaftler freue ich mich über die Möglichkeit, durch unsere Forschung das Leben eines Patienten positiv zu beeinflussen“, so Oda abschließend.
