Neue Veröffentlichungen
FDA genehmigt Bimzelx für die Behandlung von Hidradenitis
Zuletzt überprüft: 02.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
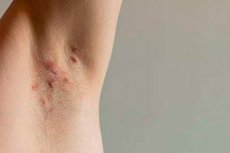
Die US-amerikanische Food and Drug Administration (FDA) hat Bimzelx (Bimekizumab-bkzx) von UCB zur Behandlung von Erwachsenen mit mittelschwerer bis schwerer Hidradenitis suppurativa zugelassen.
Bimzelx ist das erste und einzige zugelassene Medikament, das neben Interleukin 17A (IL-17A) auch selektiv Interleukin 17F (IL-17F) hemmt. Dies ist die fünfte Indikation für Bimzelx in den USA.
Grundlage für die Genehmigung:
Die Zulassung basiert auf Daten aus zwei klinischen Phase-III-Studien (BE HEARD I und BE HEARD II), die an erwachsenen Patienten mit mittelschwerer bis schwerer Hidradenitis suppurativa durchgeführt wurden.
Wichtigster Leistungsindikator:
- HiSCR50: In Woche 16 erreichte ein signifikant größerer Anteil der mit Bimzelx behandelten Patienten im Vergleich zu Placebo eine Verbesserung der Anzeichen und Symptome der Hidradenitis suppurativa um ≥50 % (gemessen am Hidradenitis Suppurativa Clinical Response (HiSCR50)-Score).
Sekundärindikator:
- HiSCR75: Das Medikament führte auch zu klinisch bedeutsamen Verbesserungen bei Patienten, die in Woche 16 im Vergleich zu Placebo eine Verbesserung von ≥75 % (HiSCR75) erreichten.
Nachhaltigkeit der Ergebnisse:
- Die klinischen Reaktionen blieben bis Woche 48 bestehen, ohne dass neue Sicherheitssignale identifiziert wurden.
Expertenmeinung:
Dr. Alexa B. Kimball, Forscherin im BE HEARD-Programm und Dermatologin am Beth Israel Deaconess Medical Center in Boston, sagte:
„Die Zulassung von Bimzelx zur Behandlung der mittelschweren bis schweren Hidradenitis suppurativa ist eine wichtige Entwicklung angesichts des erheblichen ungedeckten klinischen Bedarfs und der begrenzten Anzahl der heute verfügbaren Behandlungsmöglichkeiten.“
