Die Bedeutung des Rhythmus des Immunsystems für das Tumorwachstum
Zuletzt überprüft: 14.06.2024

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Durch die Untersuchung von Veränderungen des Immunsystems von Tumoren im Tagesverlauf zeigen Wissenschaftler der Universität Genf und der Ludwig-Maximilians-Universität München deren Auswirkungen auf die Diagnose und Behandlung von Patienten.
Die derzeit vielversprechendsten Antitumorbehandlungen sind Immuntherapien, die darauf abzielen, die Wirkung des Immunsystems des Patienten im Kampf gegen Krebs zu stärken. Obwohl diese Methoden in einigen Fällen hochwirksam sind, ist ihr Erfolg manchmal enttäuschend. Wie lässt sich diese Variabilität erklären?
In früheren Studien hat ein Team der Universität Genf (UNIGE) und der Ludwig-Maximilians-Universität München (LMU) entdeckten die Bedeutung der Rhythmik des Immunsystems für das Tumorwachstum. Dieselben Wissenschaftler haben nun gezeigt, dass das Immunprofil von Tumoren je nach Tageszeit, zu der die Biopsien durchgeführt werden, erheblich variiert.
Diese vorübergehenden Veränderungen können zu Fehldiagnosen und unzureichender Behandlung führen. Darüber hinaus könnten sich einige bisher übersehene therapeutische Ziele als Schlüssel zur Bekämpfung der Krankheit erweisen. Diese Erkenntnisse, veröffentlicht in der Zeitschrift Cell, könnten erhebliche Auswirkungen auf die klinische Versorgung und die Arzneimittelforschung haben.
Im Jahr 2022 beobachtete ein Forschungsteam unter der Leitung von Christoph Scheuermann, Professor an der Abteilung für Pathologie und Immunologie und dem Zentrum für Entzündungsforschung der Medizinischen Fakultät der UNIGE und der Universität München, ein unerwartetes Phänomen: Das Wachstum und die Schwere von Tumoren hängen mit dem zirkadianen Rhythmus der Immunzellen zusammen. „Um diese Ergebnisse jedoch in einem klinischen Kontext nutzen zu können, mussten wir ihre Details in einem realitätsnahen Modell verstehen“, sagt Scheierman.
Dazu injizierten die Wissenschaftler einer Gruppe von Mäusen Melanomzellen und sammelten die entstandenen Tumore nach zwei Wochen zu unterschiedlichen Tageszeiten. Je nach Tageszeit und damit Immunaktivierung des Tieres variierten die Anzahl der Immunzellen sowie deren Art und Eigenschaften erheblich. Dies könnte im klinischen Umfeld wichtige Auswirkungen haben.
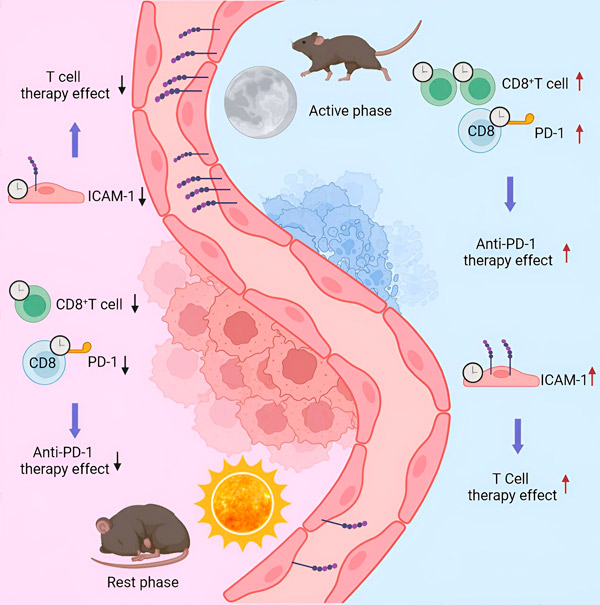
Quelle: Cell (2024). DOI: 10.1016/j.cell.2024.04.015
„Im Krankenhaus werden die Patienten einer Biopsie unterzogen, um den Tumor und seine Immuneigenschaften zu identifizieren“, erklärt Scheierman. „Auf der Grundlage dieser Untersuchung wird dann die Behandlung und insbesondere die Immuntherapie festgelegt. Nun kann die Anzahl der infiltrierten Immunzellen je nach Zeitpunkt der Biopsie sehr hoch sein – und der Tumor wird als ‚heiß‘ eingestuft – oder sehr niedrig („kalt“). Obwohl es sich um denselben Tumor handelt, kann eine Biopsie zum falschen Zeitpunkt zu einer Fehldiagnose führen.
Ein Blick auf den Zeitpunkt von Immuntherapien
Um der klinischen Realität so nahe wie möglich zu kommen, haben die Wissenschaftler bei ihren Mäusegruppen zwei zugelassene und weit verbreitete Behandlungen angewendet: CAR-T-Zellen (die speziell dafür entwickelt wurden, tumorzellspezifische Proteine zu erkennen und anzugreifen) und Immun-Checkpoint-Inhibitoren, die die natürlichen Bremsen des Immunsystems unterdrücken, um seine Aktivierung gegen Tumore zu erhöhen.
„Bei falscher Anwendung zeigten diese Behandlungen keine Wirkung.“ Zum richtigen Zeitpunkt könnte die Tumorlast deutlich reduziert werden", erklärt Scheierman. "Die Anzahl der im Tumor vorhandenen oder fehlenden Immunzellen ist ein Faktor, aber auch ihre Eigenschaften und ihr Verhalten sind wichtig."
Tatsächlich wird der Zeitpunkt ihrer Anwendung entscheidend, je nach Modulation der molekularen Elemente, die zur Entwicklung dieser Behandlungen verwendet werden. Zum richtigen Zeitpunkt werden die zu zerstörenden Zellen sofort erkannt. Zum falschen Zeitpunkt haben die Zielmoleküle eine geringere Expression und das Medikament hat keine Wirkung.
Anpassung von Behandlungsplänen und -methoden
Diese an Mäusen durchgeführten Studien werden durch Analysen der Überlebensraten von Patienten nach Immuntherapien unterstützt. Eine morgendliche Behandlung – auf dem Höhepunkt der Immunaktivierung beim Menschen – ist systematisch mit besseren Überlebensraten verbunden. Es sind Studien geplant, um die Auswirkungen von Änderungen beim Screening und Behandlungszeitpunkt auf Patienten zu bewerten. Andere Projekte werden potenzielle Medikamentenziele untersuchen, die bisher unterschätzt wurden.
Darüber hinaus haben diese Entdeckungen über Immunrhythmen noch weitreichendere Auswirkungen: zum einen aus Sicht der personalisierten Medizin Andererseits, um therapeutische Ansätze an die zeitlichen Profile der Patienten anzupassen (bei 10-20 % der Menschen stimmt der biologische Rhythmus nicht mit dem der Allgemeinbevölkerung überein) und im Zusammenhang mit anderen Pathologien, insbesondere Autoimmunerkrankungen.
