Forscher identifizieren Mutationen, die vor B-Zell-Krebs schützen
Zuletzt überprüft: 14.06.2024

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Forscher des University of Texas Southwestern Medical Center konnten Leukämie und Lymphom in einem genetisch für diese Krebsarten prädisponierten Mausmodell unterdrücken, indem sie ein Protein namens Midnolin in B-Zellen vollständig oder teilweise abbauten.
Ihre im Journal of Experimental Medicine veröffentlichten Erkenntnisse könnten zur Entwicklung neuer Behandlungen für diese Krankheiten führen, die die schweren Nebenwirkungen der derzeitigen Therapien vermeiden.
„Wir haben eine rein genetische Methode verwendet, um ein Wirkstoffziel zu finden, und dieses Ziel erwies sich als sensationell, da B-Zell-Leukämien und Lymphome in hohem Maße davon abhängig sind, während dies bei den meisten Wirtsgeweben nicht der Fall ist“, sagte Studienleiter Dr. Bruce Beutler, Direktor des Center for Genetic Host Defense und Professor für Immunologie und Innere Medizin am University of Texas Southwestern Medical Center.
Dr. Bütler, der 2011 den Nobelpreis für Physiologie oder Medizin für seine Entdeckung einer wichtigen Gruppe von Krankheitserregersensoren erhielt, die als Toll-like-Rezeptoren auf Immunzellen bekannt sind, verwendet seit langem Mutagenese – die Einführung von Mutationen in die Gene von Tiermodellen durch Einwirkung von Chemikalien. Eine Substanz namens N-Ethyl-N-Nitrosoharnstoff (ENU) als Schlüsselinstrument zur Untersuchung der Genfunktion.
Beutlers Labor hat kürzlich eine Methode namens „Automated Meiotic Mapping“ (AMM) entwickelt, die ungewöhnliche Merkmale bei mutierten Mäusen auf ursächliche Mutationen zurückführt und so Gene identifiziert, die für die Aufrechterhaltung der normalen Physiologie wesentlich sind.
Mutagenese führt häufig zur Entwicklung genetischer Krankheiten bei Tieren, was durch die Untersuchung der Anomalien bei Tieren Einblicke in die Funktion der betroffenen Gene bietet. Wie Dr. Beutler jedoch erklärte, können Mutationen auch Schutz vor Krankheiten bieten.
Beispiele sind Mutationen, die Menschen mit HIV oder Menschen mit erblicher Sichelzellenanämie vor der Entwicklung von Symptomen schützen. Die Mechanismen, die einigen schützenden Mutationen zugrunde liegen, haben die Entwicklung von Medikamenten zur Behandlung verschiedener Krankheiten inspiriert.
Auf der Suche nach schützenden Mutationen für Immunstörungen testeten Forscher mutierte Mäuse auf Immunzellen mit ungewöhnlichen Merkmalen. Bei mehreren Tiergruppen mit ungewöhnlich geringer Anzahl an B-Zellen – einem wichtigen Bestandteil des adaptiven Immunsystems, das für die Produktion von Antikörpern verantwortlich ist – verwendeten die Forscher AMM, um diesen Mangel auf Mutationen in Mynolin zurückzuführen, einem Protein, das hauptsächlich in B-Zellen vorkommt.
Obwohl Tiere, denen Midnolin vollständig fehlt, während der Entwicklung vor der Geburt sterben, haben mildere Mutationen, darunter einige, die durch genetische Techniken eingeführt wurden, bei denen das Gen im Erwachsenenalter entfernt wird, keinen erkennbaren Schaden verursacht.
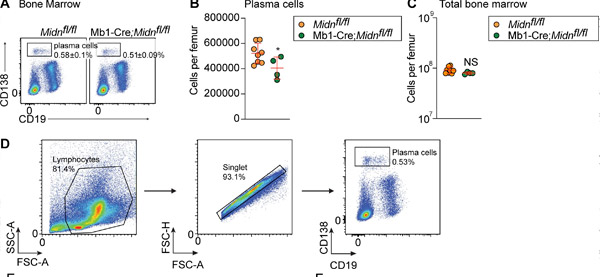
Plasmazellproduktion nach Immunisierung mit TD-Antigen-β-Galaktosidase in Mb1-Cre;Midn fl/fl-Mäusen. (A und B) Repräsentative Durchflusszytometriediagramme von (A) und Anzahl (B) von Plasmazellen im Knochenmark von 8 Wochen alten Mb1-Cre;Midn fl/fl- und Midn fl/fl-Mäusen nach Immunisierung mit β-Galaktosidase. (C) Gesamtzahl der Knochenmarkzellen pro Oberschenkelknochen. (D) Strategie zur Isolierung von Plasmazellen. Quelle: Journal of Experimental Medicine (2024). DOI: 10.1084/jem.20232132
Forscher reduzierten oder eliminierten Midnolin bei Mäusen mit genetischer Prädisposition für B-Zell-Leukämien und Lymphome, Krebsarten, bei denen sich B-Zellen unkontrolliert teilen, signifikant. Obwohl Mäuse mit normalen Midnolinspiegeln innerhalb von 5 Monaten an diesen Krankheiten starben, entwickelten die meisten Mäuse mit weniger oder keinem Midnolin nie bösartige Tumore.
Zusätzliche Experimente zeigten, dass die Rolle von Midnolin in B-Zellen darin besteht, die Aktivität von Proteasomen zu stimulieren, Zellorganellen, die beschädigte oder nicht mehr benötigte Proteine recyceln. Einige Therapien, die derzeit zur Behandlung von B-Zell-Leukämien und Lymphomen eingesetzt werden, wirken durch Hemmung der Proteasomaktivität, ähnlich wie die Midnolin-Entfernung, erklärte Dr. Beutler.
Im Gegensatz zu diesen Medikamenten, die viele potenziell schwerwiegende Nebenwirkungen haben, schien die Eliminierung oder Reduzierung von Midnolin in Tiermodellen jedoch keine negativen Folgen zu haben.
Zukünftige Forschung wird sich auf die Entwicklung von Medikamenten konzentrieren, die Midnolin hemmen, was letztendlich die Grundlage für neue Behandlungen von B-Zell-Krebs bilden könnte.
