Neue Veröffentlichungen
Aktivierung der angeborenen Immunität: ein wichtiger Teil des identifizierten Mechanismus
Zuletzt überprüft: 02.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Forscher der LMU haben das komplexe Zusammenspiel verschiedener Enzyme rund um den angeborenen Immunrezeptor Toll-like-Rezeptor 7 (TLR7) entschlüsselt, der eine wichtige Rolle bei der Abwehr von Viren spielt.
Der Toll-like-Rezeptor 7 (TLR7) auf den dendritischen Zellen unseres Immunsystems spielt eine entscheidende Rolle bei unserer natürlichen Abwehr gegen Viren. TLR7 erkennt einzelsträngige virale und andere fremde RNA und aktiviert die Freisetzung von Entzündungsmediatoren. Funktionsstörungen dieses Rezeptors spielen auch bei Autoimmunerkrankungen eine Schlüsselrolle. Daher ist es umso wichtiger, den Mechanismus der TLR7-Aktivierung zu verstehen und idealerweise zu modulieren.
Die Forscher um Professor Veit Hornung und Marlene Berouti vom Genetikzentrum München und dem Department für Biochemie der LMU konnten den komplexen Aktivierungsmechanismus genauer entschlüsseln. Aus früheren Studien war bekannt, dass komplexe RNA-Moleküle zerschnitten werden müssen, damit der Rezeptor sie erkennen kann.
Mithilfe verschiedener Technologien, von der Zellbiologie bis zur Kryo-Elektronenmikroskopie, haben LMU-Forscher die Verarbeitung einzelsträngiger Fremd-RNA zur Erkennung von TLR7 aufgeklärt. Ihre Arbeit wurde in der Fachzeitschrift Immunity veröffentlicht.
Zahlreiche Enzyme sind an der Erkennung fremder RNA beteiligt
Im Laufe der Evolution hat sich das Immunsystem darauf spezialisiert, Krankheitserreger anhand ihres genetischen Materials zu erkennen. Beispielsweise wird der angeborene Immunrezeptor TLR7 durch virale RNA stimuliert. Man kann sich virale RNA als lange Molekülstränge vorstellen, die zu groß sind, um als Liganden für TLR7 erkannt zu werden. Hier kommen Nukleasen ins Spiel – molekulare Schneidewerkzeuge, die den RNA-Strang in kleine Stücke zerschneiden.
Endonukleasen zerschneiden die RNA-Moleküle wie eine Schere in der Mitte, während Exonukleasen den Strang von einem Ende zum anderen spalten. Dabei entstehen unterschiedliche RNA-Fragmente, die nun an zwei verschiedene Bindungstaschen des TLR7-Rezeptors binden können. Erst wenn beide Bindungstaschen des Rezeptors mit diesen RNA-Stücken besetzt sind, wird eine Signalkaskade ausgelöst, die die Zelle aktiviert und in einen Alarmzustand versetzt.
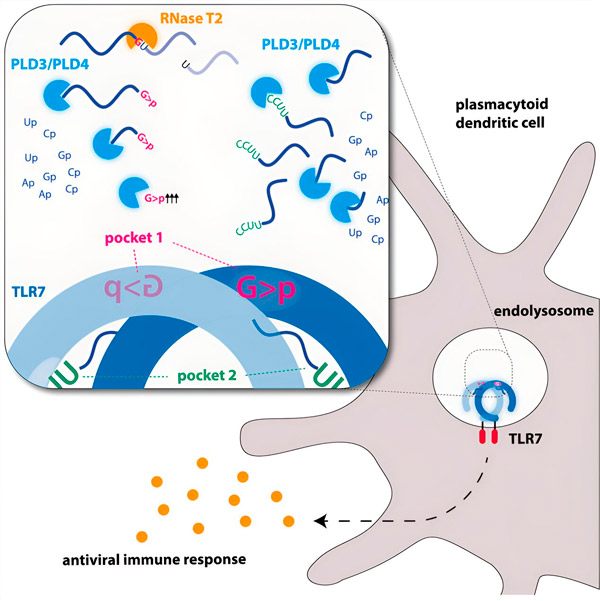
Grafik. Quelle: Immunity (2024). DOI: 10.1016/j.immuni.2024.04.010
Die Forscher fanden heraus, dass die RNA-Erkennung durch TLR7 die Aktivität der Endonuklease RNase T2 erfordert, die zusammen mit den Exonukleasen PLD3 und PLD4 (Phospholipase D3 und D4) wirkt. „Es war zwar bekannt, dass diese Enzyme RNA abbauen können“, sagt Hornung, „aber wir haben nun gezeigt, dass sie mit TLR7 interagieren und es dadurch aktivieren.“
Ausgleich des Immunsystems
Die Forscher fanden außerdem heraus, dass PLD-Exonukleasen in Immunzellen eine Doppelrolle spielen. Im Fall von TLR7 wirken sie entzündungsfördernd, während sie im Fall eines anderen TLR-Rezeptors, TLR9, entzündungshemmend wirken. „Diese Doppelrolle der PLD-Exonukleasen deutet auf ein fein abgestimmtes Gleichgewicht bei der Kontrolle der richtigen Immunantwort hin“, erklärt Berouti.
„Die gleichzeitige Stimulierung und Hemmung der Entzündung durch diese Enzyme könnte ein wichtiger Schutzmechanismus sein, um Fehlfunktionen des Systems vorzubeugen.“ Welche Rolle weitere Enzyme in diesem Signalweg spielen und ob sich die beteiligten Moleküle als Zielstrukturen für eine Therapie eignen, sei Gegenstand weiterer Forschung.
