Neue Veröffentlichungen
FDA genehmigt erste cremeförmige Behandlung für chronisches Handekzem
Zuletzt überprüft: 27.07.2025

Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
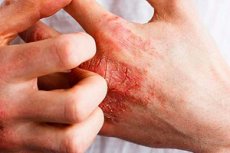
Die US-amerikanische Food and Drug Administration (FDA) hat die erste Creme zugelassen, die speziell zur Behandlung von chronischem Handekzem (CHE) entwickelt wurde.
CHE ist eine häufige Erkrankung, die durch rote, juckende, rissige Haut an Händen und Handgelenken gekennzeichnet ist.
Anzupgo (Delgocitinib-Creme) ist für Erwachsene mit mittelschwerem bis schwerem CHE zugelassen, die keine topischen Steroide anwenden können oder bei denen diese unwirksam sind.
„Die Zulassung von Anzupgo bestätigt unser Engagement, in schwer behandelbare Hautkrankheiten zu investieren, um Patienten dort neue Behandlungsmöglichkeiten zu bieten, wo der Bedarf am größten ist“, sagte Christophe Bourdon, CEO von LEO Pharma, dem Hersteller von Anzupgo, in einer Pressemitteilung.
Im Gegensatz zur atopischen Dermatitis, der häufigsten Form von Ekzemen, ist CHE eine seltene und schwächende Erkrankung. Laut der National Eczema Association betrifft sie etwa 10 % der US-Bevölkerung und dauert länger als drei Monate oder flammt mindestens zweimal im Jahr auf.
Anzupgo wirkt, indem es JAK-Enzyme blockiert, die Entzündungen verursachen, die wiederum Schübe von Handekzemen auslösen.
Genetische Veranlagung sowie der Kontakt mit Reizstoffen und Allergenen können zur Entwicklung dieser Form von Ekzem führen. Besonders gefährdet sind Menschen in Branchen wie Reinigung, Friseurhandwerk und Gesundheitswesen, wo sie häufiger mit Chemikalien in Kontakt kommen und darauf reagieren.
Untersuchungen zeigen, dass diese Krankheit schwerwiegende Auswirkungen auf die Lebensqualität und die psychische Gesundheit einer Person hat.
Ein Dermatologe aus Detroit lobte die Entscheidung der FDA.
„In meiner Zeit als Dermatologin habe ich aus erster Hand gesehen, wie sehr Patienten unter dem Juckreiz und den Schmerzen im Zusammenhang mit CHE leiden und wie sehr sie ihren Alltag beeinträchtigen“, sagte Dr. Linda Stein Gold, Leiterin der klinischen Forschung bei Henry Ford Health in Detroit, in einer Pressemitteilung von LEO Pharma US. „Ich bin überzeugt, dass diese neue Behandlungsoption von Dermatologen begrüßt wird, die nach wirksamen und sicheren Wegen zur Behandlung dieser Symptome suchen.“
Studien, die vor der FDA-Zulassung durchgeführt wurden, zeigten, dass Patienten mit Handekzemen, die die Creme anwendeten, häufiger eine Besserung erfuhren als diejenigen, die ein Placebo oder eine Scheincreme verwendeten. Das Medikament trägt nicht den schwarzen Warnhinweis, der für andere topische und orale JAK-Hemmer erforderlich ist.
„Wir sind begeistert, dass die FDA die Auswirkungen erkannt hat, die mittelschweres bis schweres chronisches Handekzem auf Patienten hat“, sagte Christine Belleson, CEO und Präsidentin der National Eczema Association, in einer Pressemitteilung.
„Für Menschen mit dieser schwächenden Hauterkrankung an den Händen ist es extrem schwierig; sie beeinträchtigt ihre Arbeitsfähigkeit, den Kontakt zu anderen und den Kontakt zu den Menschen, die ihnen wichtig sind“, fügte sie hinzu. „Diese Unterstützung gibt der Neurodermitis-Gemeinschaft und allen, die nach dauerhafter Linderung ihrer verheerenden Symptome suchen, Hoffnung und Perspektive.“
Die Creme ist bereits in der Europäischen Union, Großbritannien, der Schweiz und den Vereinigten Arabischen Emiraten zugelassen.
